0 引言
1 分离流程
1.1 流程设计
1.2 基本模块
1.2.1 压缩机模块
1.2.2 水合物生成/解离反应器

1.2.3 制冷系统
2 结果与讨论
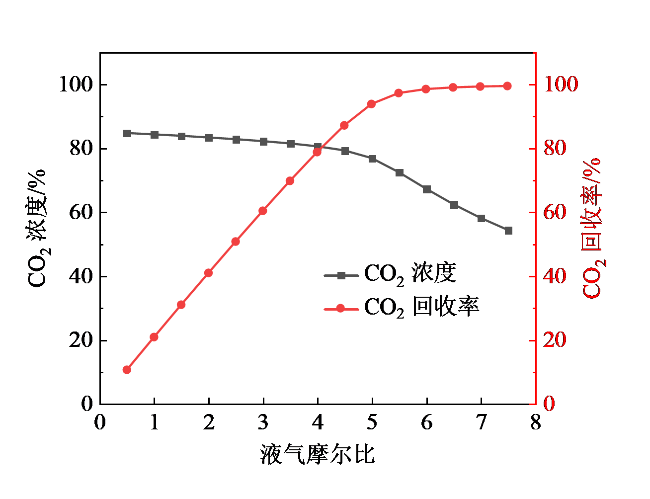
2.1 液气摩尔比对分离过程的影响
图4 液气摩尔比对CO2分离效果的影响Fig. 4 Influence of liquid/gas molar ratio on CO2 separation efficiency |
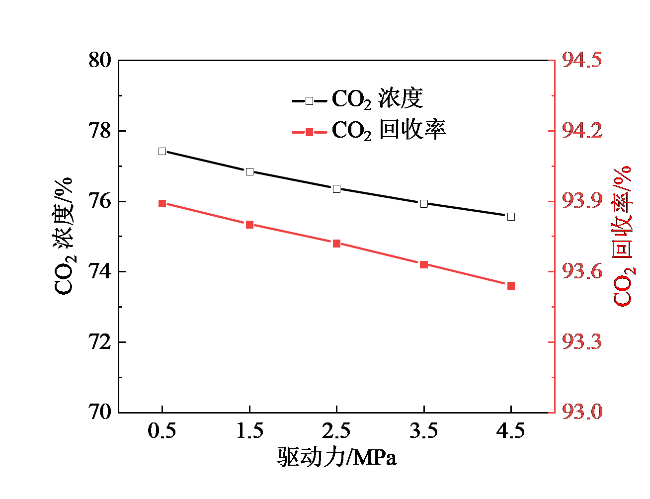
2.2 驱动力对分离过程的影响
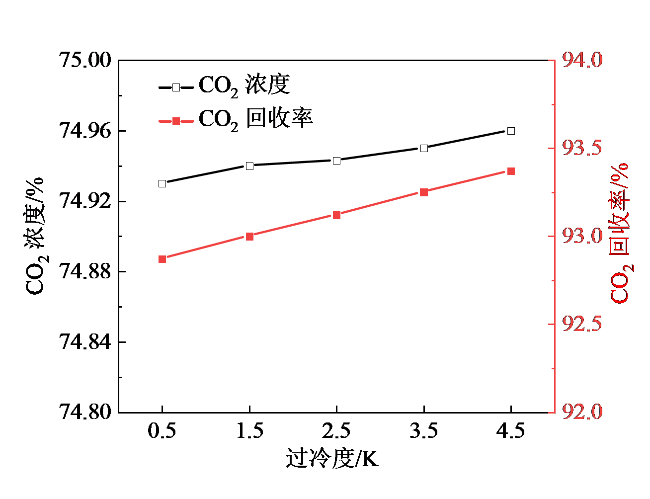
2.3 过冷度对分离过程的影响
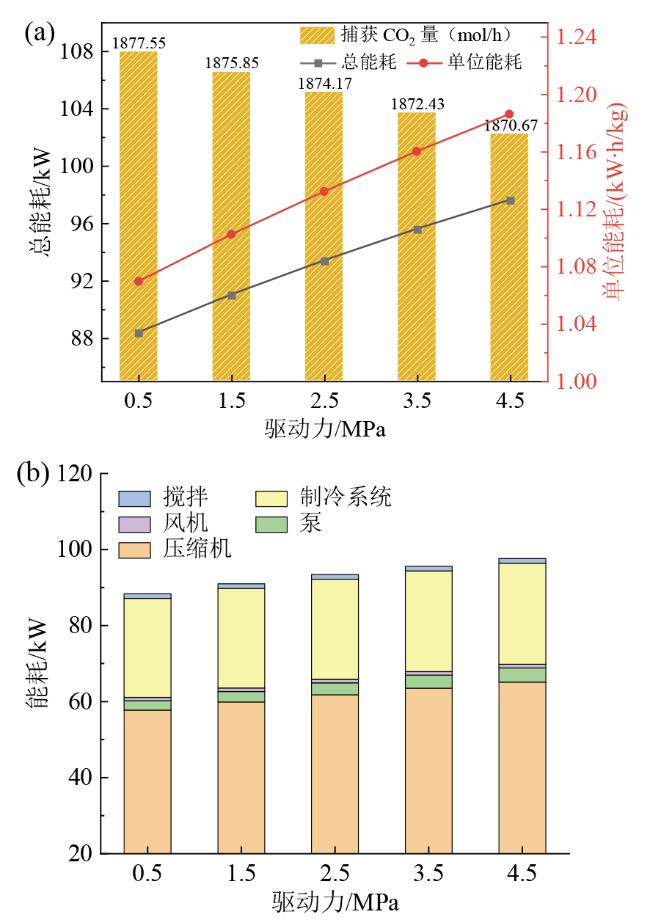
2.4 CO2比例对能耗的影响
2.5 不同反应条件能耗对比
表1 不同反应条件的水合物法分离结果Table 1 Separation results of hydrate method under different reaction conditions |
| 分离条件 | CO2浓度/ % | CO2流量/ (mol/h) | CO2回收率/ % | 压缩机能耗/ kW | 泵能耗/ kW | 风机能耗/ kW | 制冷系统能耗/ kW | 搅拌能耗/ kW | 单位能耗/ (kW∙h/kg) |
|---|---|---|---|---|---|---|---|---|---|
| 274 K/0.5 MPa | 77.40 | 1 877.55 | 93.90 | 57.76 | 2.46 | 0.90 | 26.05 | 1.18 | 1.07 |
| 278 K/0.5 MPa | 74.90 | 1 857.34 | 92.90 | 67.85 | 4.30 | 0.89 | 24.64 | 1.18 | 1.21 |