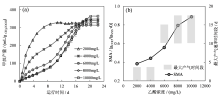作者简介:姜萌萌(1992-),女,博士研究生,主要从事厌氧膜生物反应器与废弃物资源化处理研究。乔 玮(1979-),男,博士,教授,主要从事废水和废弃物的厌氧生物处理研究。
在高温 (50±1)℃条件下处理实际工程的餐厨垃圾,采用全混式厌氧反应器(CSTR)进行了80 d的连续试验。试验以水力停留时间(HRT)20 d启动,HRT 15 d连续运行,研究了反应器启动和运行期间的发酵特性,解析了餐厨垃圾厌氧消化运行稳定性和代谢活性。试验结果表明,在HRT 15 d、有机负荷(OLR)为7.3 kgCOD/(m3∙d)的条件下,容积产甲烷率为2.2 L/(L∙d),挥发性固体(VS)的甲烷产率达到480 L/kgVS左右,有机物转化率约为95%。批次试验表明,高温产甲烷菌代谢乙酸能力较强,在适宜pH下可承受10 000 mg/L的乙酸浓度。餐厨垃圾的高温降解速率快,10 d达到90%的产气,有承受更高负荷的可能。系统pH稳定在7.6 ~ 7.7,总氨氮和自由氨浓度低于抑制水平。研究结果表明,餐厨垃圾的高温厌氧消化可实现较高的产气潜力和有机物去除率,系统稳定性好且有机物转化效率高,具有应用于工程高温餐厨垃圾厌氧处理的潜力。
In this research, the actual food waste was used for anaerobic digestion (AD) under the condition of thermophilic (50±1)oC in a continuous stirred tank reactor (CSTR), starting with a hydraulic retention time (HRT) of 20 days, and operating with HRT of 15 days for a total of 80 days. The fermentation characteristics during startup and operation of the reactor, and the operational stability and metabolic activity of AD of food waste were studied. Results showed that under the condition of an HRT of 15 days and an organic load rate (OLR) of 7.3 kgCOD/(m3∙d), the volumetric methane production rate was 2.2 L/(L∙d), and the methane yield reached to 480 L/kgVS. The organic conversion rate was about 95%. Thermophilic methanogens had a strong ability to metabolize acetic acid and can withstand 10 000 mg/L of acetic acid at a suitable pH value. The degradation rate of the food waste under thermophilic temperature was fast, and it took about 10 days to reach 90% of the methane production, it was possible to withstand higher OLR under this condition. The pH value of the system was stable at 7.6 - 7.7; the total ammonia nitrogen (TAN) and free ammonia (FAN) were below the inhibition level. The results showed that thermophilic AD of food waste can achieve higher biogas production and organic matter removal rate, with good system stability and high conversion efficiency. The thermophilic AD of food waste has the possibility to be applied in engineering.
开放科学(资源服务)标识码(OSID): 
随着垃圾分类政策的实施, 厨余垃圾分出量激增, 后端处理难度增加[1]。以食品加工、饮食服务和单位供餐为主的餐厨垃圾经过分选和除油后, 悬浮物和易降解有机物含量高, 是目前处理的难点。据不完全统计, 国内约一半以上的餐厨垃圾处理工程采用厌氧消化工艺[2]。厌氧消化可以将有机物转化为生物能源, 广泛应用在废水和废弃物的处理中, 是当前餐厨垃圾处理的主流技术。目前餐厨垃圾厌氧处理工程多数为中温消化, 但餐厨垃圾经高温除油后冷却到中温进行发酵的工艺复杂且高温能量没有得到充分利用, 对现有工艺并不合理。若能在高温除油后直接在高温条件下进行厌氧发酵处理, 既可省去物料的冷却降温过程, 简化其工艺, 同时也能提高处理效率和处理负荷, 对实际工程具有重要意义。有研究表明, 餐厨垃圾除油后进行厌氧消化, 产气潜能和产甲烷速率均显著提高, 且高温处理餐厨垃圾比中温处理的产气量高[3, 4, 5, 6], 可提高运行过程中的有机负荷[7]。但也有研究报道在高温条件下餐厨垃圾厌氧消化存在稳定性差的问题, 挥发性脂肪酸(volatile fatty acid, VFA)积累和产气降低等在连续运行过程中更容易发生[8, 9]。挥发性脂肪酸、有机负荷(organic loading rate, OLR)和微量元素等均是影响餐厨垃圾发酵稳定性的重要因素。目前, 对于餐厨垃圾的研究多集中在连续试验中高温的特性比较、有机负荷的影响和两相厌氧等[5, 10, 11], 针对物质流动和微生物活性等基础方面的分析和研究较少。
本研究采用全混式厌氧消化反应器(continuous stirred tank reactor, CSTR), 在高温50℃条件下处理实际餐厨垃圾处理工程收集并预处理后的餐厨垃圾, 研究其连续运行性能和处理过程中的物质转化和污泥代谢活性。此外, 通过产甲烷潜能从基础层面研究了餐厨垃圾的产气潜力, 为高温餐厨垃圾厌氧消化工艺提供理论基础。
接种污泥取自北京市某市政污泥厌氧处理工程正常运行的中温市政污泥发酵罐, 首先置于中温 35℃水浴中2 d, 之后每天升高5℃培养, 共升温3 d, 在达到50℃后再维持该温度4 d完成活化过程, 稀释两倍后用于接种。餐厨垃圾取自江苏省某餐厨垃圾处理公司, 经分拣、破碎、制浆、高温除油和三相分离处理后, 取液相餐厨垃圾保存在4℃条件下供研究使用。进料中补充一定浓度的微量元素[12]。餐厨垃圾与接种污泥(稀释两倍后)性质见表1。
| 表1 原料与接种污泥的基本性质 Table 1 Characteristics of food waste and inoculum |
TS、VS、MLSS和VSS的测定采用重量法[13], pH用梅特勒-托利多酸度计(FE 20, 瑞士)测定。TCOD和SCOD采用连华试剂盒和消解仪(哈希, DRB 200, 美国)消解后用分光光度计(哈希, DR2800, 美国)在610 nm吸光度下检测, 以葡萄糖为标准样品; 氨氮(TAN)采用纳氏试剂比色法测定; 碱度采用滴定法[14]测定。蛋白质采用Lowry法测定, 以牛血清白蛋白为标准样品, 碳水化合物的测定为苯酚-硫酸法, 以葡萄糖为标准样品, 具体步骤参照文献[10]。粗脂肪含量测定依据索氏抽提法。沼气产量由湿式气体流量计(LMF-2, 北京金志业仪器设备有限公司)读数变化得出, 沼气成分(CH4与CO2)采用气相色谱仪(GC-8A, 日本岛津)测试, 采用13X分子筛柱, 柱温50℃, 进样口与检测器温度为120℃。VFA检测采用气相色谱仪(GC-2010 Plus, 日本岛津)测试, 采用30 m × 0.25 mm × 0.25 μ m的毛细柱和热导检测器(thermal conductivity detector, TCD), 载气(氮气)分压为0.5 MPa, 氢气流速20 ~ 30 mL/min, 进样口、柱温和火焰离子化检测器(flame ionization detector, FID)温度分别设置为230℃、60℃和250℃, 进样体积为1 μ L。
自由氨(free ammonia nitrogen, FAN)的计算依据文献[15]中的公式:
$\text{FAN}=\frac{{{10}^{\text{pH}}}}{\exp \left( \frac{6334}{T} \right)+{{10}^{\text{pH}}}}\times \text{TAN}$ (1)
式中:自由氨FAN和总氨氮TAN的单位均为g/L; T为厌氧消化温度, K; pH为发酵液中的酸度值。
有机物转化效率和有机物去除率分别用式(2)和式(3)表示。
${{C}_{\text{COD}}}=\frac{\text{CO}{{\text{D}}_{\text{C}{{\text{H}}_{4}}}}+\text{CO}{{\text{D}}_{\text{M}}}}{\text{CO}{{\text{D}}_{\text{in}}}}\times 100\text{ }\!\!%\!\!\text{ }$ (2)
式中:${{C}_{\text{COD}}}$为COD转化率; $C\text{O}{{\text{D}}_{\text{C}{{\text{H}}_{4}}}}$为气体中甲烷的COD, $\text{CO}{{\text{D}}_{\text{M}}}$为转化为微生物的COD, $\text{CO}{{\text{D}}_{\text{in}}}$为进料中的COD, 单位均为g。其中, $\text{CO}{{\text{D}}_{\text{M}}}$按文献[16]中每转化1 g COD生成0.08 g微生物进行计算, 即转化系数为0.08 gVSS/gCOD。进料总COD为气体中甲烷COD、微生物增殖消耗COD和未转化部分的COD之和。
$R=\frac{{{M}_{\text{in}}}-{{M}_{\text{out}}}}{{{M}_{\text{in}}}}\times 100\text{ }\!\!%\!\!\text{ }$ (3)
式中:$R$为有机物去除率; M代表有机物(TS、VS、COD、蛋白质、碳水化合物和脂质等); ${{M}_{\text{in}}}$和${{M}_{\text{out}}}$分别为进料和出料中的COD, g/L。
在水力停留时间(hydraulic retention time, HRT)15 d运行稳定期, 取出料污泥作为接种, 餐厨垃圾作为原料进行产甲烷潜能批次试验。其中, 出料污泥需先放入高温 (50 ± 1)℃水浴锅中3 d以降低产气背景值。批次试验装置是总容积为120 mL的血清瓶, 首先向血清瓶中加入70 mL接种污泥, 再加入1 g TCOD餐厨原料, 通入氮气30 s后盖上瓶塞, 并用铝盖压紧, 标号后置于恒温震荡水浴箱中。试验分为实验组和空白对照组, 各设置了两个平行。根据产气量每1 ~ 3 d使用玻璃注射器测沼气产量, 并采用气相色谱测试甲烷含量。累积产气量值用修正的Gompertz模型拟合得到, 如式(4)所示:
$P={{P}_{0}}\exp \left\{ -\exp \left[ \frac{{{R}_{\max }}\text{e}}{{{P}_{\text{0}}}}\left( \lambda -t \right)+1 \right] \right\}$ (4)
式中:P为t时刻的累积产气量, mL; P0为产甲烷潜能, mL; Rmax为最大产甲烷速率, mL/d; λ 为产气迟滞期, d; t为试验持续时间, d。
取HRT 15 d运行期间第80 d的新鲜出料进行试验。在总容积120 mL血清瓶中进行, 依次加入90 mL大量元素与微量元素配制的缓冲溶液[15]、10 mL新鲜出料污泥和不同浓度的乙酸溶液, 形成不同乙酸的浓度(0 mg/L、2 000 mg/L、4 000 mg/L、6 000 mg/L、8 000 mg/L和10 000 mg/L), 每个浓度做2个平行。向发酵瓶内充入N2, 排出氧气, 盖上瓶塞, 并用铝盖压紧, 标号后置于水浴箱中。根据产气量, 每1 ~ 3 d使用玻璃注射器测沼气日产量。
比产甲烷活性(specific methanogenic activity, SMA)计算式为:
$\text{ }SMA=\frac{1}{\text{VSS}\cdot {{V}_{\text{R}}}f}\cdot \frac{\text{d}{{V}_{\text{C}{{\text{H}}_{\text{4}}}}}}{\text{d}t}$ (5)
式中:SMA为比产甲烷活性; ${{V}_{\text{C}{{\text{H}}_{\text{4}}}}}$为累积产甲烷量, mL; ${{V}_{\text{R}}}$为血清瓶中添加的污泥量, L; f为COD与甲烷产量的转化系数, 350 mL/gCOD; VSS为所用污泥的挥发性悬浮固体含量, g/L; t为时间, d。
试验反应器总容积2 L, 有效容积1.8 L, 接种1.8 L污泥进行试验, 在试验开始时按照HRT 20 d, 每天进行一次手动进出料。反应器为全混搅拌, 由亚速旺(TMK-2K, 日本)加热头保持 (50± 1)℃恒温水循环, 产生的气体收集在气袋中, 每日测试气体成分后用湿式气体流量计记录产气量。试验以HRT 20 d启动, HRT 15 d运行, 共运行80 d。
图1反映了启动和运行期间的产气(图1a、图1c和图1e)和运行稳定性(图1b、图1d和图1f)指标随时间的变化, 并在表2中进行了总结。在启动运行期间(HRT 20 d), 将OLR从4.2 kgCOD/(m3∙ d) 提高到5.4 kgCOD/(m3∙ d), 容积产甲烷率提高到1.6 L/(L∙ d), 甲烷含量稳定在59%左右。之后, 将HRT缩短到15 d后运行了54 d, OLR为7.3 kgCOD/(m3∙ d), 容积产沼气率和容积产甲烷率分别稳定在3.9 L/(L∙ d) 和2.2 L/(L∙ d), 每升餐厨垃圾可以产生约58 L沼气, 其中甲烷含量为58%左右。此外, 在HRT 15 d, 单位COD产甲烷量约为0.31 L/gCOD, 单位进料的VS产甲烷量约0.48 L/gVS, VS产量与XIAO等[17]和ALGAPANI等[10]的研究结果相近, 比LIU等[5]和YIRONG等[18]的高6% ~ 17%。表明高温条件下餐厨垃圾厌氧消化可在一个月内成功启动且稳定运行。
| 表2 连续试验在不同HRT下的运行性能总结 Table 2 Summary of the CSTR operation performance under different HRTs |
由图1b可见, HRT 20 d和HRT 15 d运行期间的pH相差不大, 分别为7.7和7.6。在该pH条件下, 整个运行阶段的总碱度在6.7 ~ 7.7$\text{ }{{\text{g}}_{\text{CaC}{{\text{O}}_{\text{3}}}}}$/L, 碳酸氢盐碱度在3.0 ~ 3.6$\text{ }{{\text{g}}_{\text{CaC}{{\text{O}}_{\text{3}}}}}$/L。在启动初期, VFAs浓度约100 mg/L, 提升OLR至5.4 kgCOD/(m3∙ d) 并运行一段时间后, VFAs基本在 (47 ± 5) mg/L, 主要为乙酸, 浓度为 (47 ± 5) mg/L。HRT 15 d后期, VFAs浓度比HRT 20 d期间高, 为 (135 ± 23) mg/L, 主要为乙酸和丙酸, 浓度分别为 (80 ± 20) mg/L和 (54 ± 25) mg/L。
有研究报道氨氮是影响餐厨垃圾厌氧消化稳定性的因素之一[18, 19], 且FAN被认为是氨抑制产生的主要原因[20, 21], 可渗透到细胞内部, 导致质子失衡, 改变细胞内的pH。厌氧消化驯化后微生物对FAN的耐受浓度可达到337 ~ 800 mg/L[20, 22]。从HRT 20 d缩短到HRT 15 d的过程中, TAN增加约106 mg/L, 但在80 d的运行过程中TAN低于2 000 mg/L, 低于文献报道的发酵抑制阈值2 500 ~ 3 500 mg/L[23, 24]。本研究发酵系统启动期和稳定期FAN分别为 (156 ± 2) mg/L和 (163 ± 11) mg/L, 均远低于文献报道的中高温FAN产气抑制浓度[6, 20], 结合TAN浓度分析表明系统未明显受到氨抑制。
为进一步考察餐厨垃圾在高温条件下的产气特性, 采用批次试验进行产甲烷潜能研究。由图2a可知, 发酵40 d后, 餐厨垃圾最大产沼气量为700 mL/gCOD, 最大产甲烷量为270 mL/gCOD, 由Gompertz模型拟合出的最大产沼气量和甲烷量分别为653 mL/gCOD和250 mL/gCOD, 拟合相关系数分别为0.910和0.931, 与实际吻合较好。根据表1, 本研究中TCOD/VS约为1.6, 则每克VS实际产甲烷量约为426 mL/gVS, 该研究结果与苏敏等[3]以除油餐厨垃圾在高温条件下的潜能试验十分接近, 比王延昌等[25]在高温条件下处理餐厨垃圾产气潜能略高, 可能是由于本研究中餐厨垃圾在处理前经过了高温处理和高度破碎, 有机质更易降解; 而连续试验中微量元素的添加可能是单位VS产气率高于批次试验的因素之一。
对实际甲烷产量的分析见图2b, 日产气峰值在1 d内出现, 为143 mL/gCOD, 之后逐渐下降。1 d内即可达到总产气量的40%, 约10 d可达到总产气的90%, 说明餐厨垃圾降解和产气较快。约3 d内完成快速发酵, 与刘月玲等[26]以实际餐厨垃圾进行高温潜能试验研究结果相近。在高温连续发酵处理中, HRT 15 d为相对理想的HRT, 且有将HRT进一步缩短的可能。
污泥的乙酸比产甲烷活性反映了污泥对COD的去除以及产甲烷的能力, 可反映厌氧污泥的品质。同时, 为了研究发酵污泥对不同浓度乙酸的分解特性, 本研究采用2 000 ~ 10 000 mg/L的乙酸浓度进行污泥的产甲烷活性试验。图3a给出了不同乙酸浓度条件下, 单位乙酸的连续产气测试曲线, 当乙酸浓度为2 000 mg/L时, 7 d内基本完成产气, 当乙酸浓度为4 000 mg/L, 在5 d内能够迅速产气, 约20 d完成产气, 产甲烷菌对4 000 mg/L以下的乙酸浓度代谢能力较强。当乙酸浓度为6 000 ~ 10 000 mg/L, 产气呈明显的两段特征, 甲烷产量从10 d后开始明显增加, 之后乙酸能被快速降解。LI等[27]在咖啡渣的中高温厌氧处理中, 采用1 000 ~ 10 000 mg/L的乙酸浓度测试污泥活性, 随着乙酸浓度的增加, 产气延迟期也增加。
图3b总结了不同乙酸浓度条件下的SMA, 2 000 mg/L乙酸浓度下的SMA为0.38 gCOD/(gVSS∙ d), 比KUMAR等[7]在高温条件下和李蕾等[28]在中温条件下的研究结果[0.11 ~ 0.27 gCOD/(gVSS∙ d)]略高; 此外, KUMAR等研究中也表明, 高温餐厨垃圾厌氧发酵的SMA和产气性能比中温更好。随着乙酸浓度的增加, SMA逐渐升高, 在10 000 mg/L的乙酸浓度条件下达到0.89 gCOD/(gVSS∙ d), 但结合图3a, 在该厌氧消化系统中污泥对乙酸的承受能力可达10 000 mg/L, 但在大于4 000 mg/L的浓度条件下, 微生物需要一定的时间适应。
图4是启动与运行期间进出料的TCOD和VS变化以及HRT 15 d稳定运行阶段的有机物去除率和COD的平衡。运行期间的进料TCOD为105 ~ 112 g/L, 出料TCOD基本稳定在20 ~ 22 g/L, 去除率约为82%; 进、出料VS浓度分别约为63 ~ 70 g/L和10 ~ 14 g/L, 去除率为83%。本研究中TCOD去除率比ALGAPANI等[10]研究中OLR为10 kgCOD/(m3∙ d)条件下的TCOD去除率高约11%, 与XIAO等[17]报道的结果相近。
 | 图4 有机质浓度变化、HRT 15 d的有机物去除率和基于COD的物料平衡Fig. 4 Organic matter variation, removal efficiencies and COD mass balance under HRT 15 days |
在碳水化合物和脂肪去除率方面, 均能达到95%以上, 而蛋白质的降解较差, 其去除率仅为50%左右。据报道, 厌氧消化中的氨氮主要来源于蛋白质分解[29], 该研究中较低的氨氮浓度可能与蛋白质降解率相关。由图4d可知, 不溶性COD约占进料总TCOD的40%, 而SCOD占比60%, SCOD高占比可能是餐厨垃圾在反应器中快速降解的原因之一; 出料COD中, VFA-COD仅占0.15%, 约83%为甲烷, 溶解性COD比例为4.5%。采用50℃高温处理实际餐厨垃圾可实现较为理想的机物去除率。
图5进一步分析总结了HRT 15 d运行过程中的COD物质转化和物质流动, 根据图5a, 在餐厨垃圾COD的转化过程中, 约95%的有机物可被微生物利用转化, 其中85%被转化生成甲烷, 10%被用于厌氧微生物的增殖, 未降解的有机物占5%, 与COD物料平衡中的结果对应。由图5b可知, 虽然进料总VFA较低, 仅为2 g/L左右, 出料中仍含有少量VFA, 但对发酵几乎没有影响。进料TCOD较高, 约为110 g/L, 且去除率约达82%, 说明餐厨垃圾中的碳源在高温厌氧消化过程中可有效被代谢, 在甲烷产生过程中贡献较大。
(1)餐厨垃圾在高温条件下进行厌氧消化, 可实现快速启动和正常运行。在补充一定量微量无机营养元素的条件下, 有机物的转化率达到95%, 有机酸残留浓度低, 证明餐厨垃圾高温厌氧消化工艺既有很高的效率, 又能维持很好的稳定性, 是可以工程化应用的工艺。
(2)长期连续运行试验证明, 在高温厌氧系统中甲烷菌对乙酸具有很强的代谢活性, 氨氮和自由氨均未对高温菌群产生抑制作用, 表明高温厌氧工
艺具有良好的环境耐受性。
(3)结合连续试验的工艺运行性能和原料产甲烷潜能的试验结果, 高温厌氧工艺具有缩短HRT进而提高工艺负荷的空间, 在保障处理效率的前提下, 进一步提高处理能力。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|