作者简介:刘书畅(1997-),男,硕士研究生,主要从事聚合物电解质方面的研究。张灵志(1969-),男,博士,研究员,博士生导师,长期从事有机/高分子光电功能材料和纳米材料的合成、制备及其在光电和电化学储能器件应用方面的研究。
锂离子电池已广泛应用于便携式电子设备和电动汽车等领域,然而商用锂离子电池中含有大量易燃的碳酸酯类有机溶剂,容易造成安全隐患。离子液体具有蒸汽压低、化学结构设计多样性、热稳定性及电化学稳定性优异等优点,可以用来代替易燃有机溶剂,在电化学储能领域具有广阔的应用前景。聚离子液体是一类聚合物重复单元上含有阴、阳离子的新型聚合物电解质材料,兼具离子液体和聚合物固态电解质不漏液、易于加工的优势。根据离子液体和聚离子液体化学结构的设计合成及其在锂离子电池中的应用形式,综述了近年来离子液体电解质的研究进展,并提出了离子液体电解质未来的应用挑战和发展方向。
Lithium-ion batteries have been widely used in portable electronic devices and electric vehicles. However, the commercial electrolytes used in lithium-ion batteries are flammable due to the low flash point of carbonic ester which often causes safety hazards in practical applications. Ionic liquids hold great potential as alternative safe electrolytes to the volatile organic solvents in the conventional liquid electrolytes for lithium-ion batteries, owing to their unique advantages such as low vapor pressure, excellent chemical stability, and thermal stability. Poly(ionic liquid)s possess both advantages of ionic liquids and solid polymer electrolytes such as no electrolyte leakage and ease of processing in the production of batteries. In this article, the recent progress in the synthesis and the application of ionic liquids and poly(ionic liquid)s as electrolytes for lithium-ion batteries were reviewed. The application challenges and the development directions of these ionic liquid electrolytes were also presented.
锂离子电池相对于其他二次电池, 具有较高的工作电压、能量密度和更长的循环寿命, 这些优点使其成为最具发展前景的电池[1, 2]。传统的锂离子电池含有大量易燃的有机溶剂, 在锂离子电池生产应用中存在安全隐患[3, 4], 随着锂离子电池在便携式电子设备、电动汽车等领域的广泛使用, 研发更高安全性的锂离子电池引起了人们的广泛关注[5, 6, 7]。离子液体具有蒸汽压低、结构可设计、优异的热稳定性及电化学稳定性和不易燃等优点; 聚离子液体继承了离子液体的部分优点, 同时又兼具聚合物无漏液、易于加工等优势。近年来, 离子液体在锂离子电池电解质领域展现出了令人欣喜的应用潜力[8]。
离子液体是由有机阳离子和无机/有机阴离子组成, 在室温或接近室温条件下呈液态的离子化合物[9]。可以按照组成离子液体的阴阳离子结构不同对离子液体进行分类, 离子液体中常见的阴阳离子化学结构列于图1。
以离子液体中阳离子结构不同来划分, 离子液体可分为咪唑类、吡啶类、哌啶类、吡咯烷类、季铵盐类、季膦盐类等[10]。
1.1.1 吡啶类
吡啶类离子液体是一种含有一个氮原子的不饱和六元环, 是最早研究的一类离子液体。1948年, HURLEY[11], WIER等[12, 13]制备了无色透明的N-烷基吡啶类氯铝酸盐离子液体, 为第一代离子液体。但由于大部分吡啶类离子液体的熔点较高, 黏度较大, 其在电化学器件方面的应用受到一定限制。DILEO等[14], 将一系列咪唑类和吡啶类离子液体与碳酸酯类溶剂混合得到电解液, 测得在同等条件下, 吡啶类离子液体的离子电导率均低于咪唑类离子液体。GUPTA等[15]制备了含1-丁基-3-甲基吡啶鎓双三氟甲磺酰亚胺盐(B1M3Py-TFSI)的聚环氧乙烷(polyethylene oxide, PEO)基聚合物电解质, 热分解温度达到376℃, 但常温离子电导率仅为2.54 × 10-5 S/cm。
1.1.2 咪唑类
咪唑类离子液体是研究最多的离子液体, 1992年WILKES等[16]首次报道制备了一种在空气和水分条件下保持稳定的离子液体1-乙基-3-甲基咪唑四氟硼酸盐(EtMeim-BF4), 是第二代离子液体的开端。咪唑类离子液体是一种含有两个氮原子的不饱和五元环, 这种特殊结构使正电荷在N-C-N之间离域, 降低了阳离子与阴离子之间的相互作用, 使得其具有低黏度、低熔点和较高的离子电导率。然而, 咪唑类离子液体的C-2位很容易被酸质子化, 在锂离子电池中, C-2位很容易在阳极上发生还原反应, 将C-2位上的氢用烷烃取代可以降低C-2位质子化的还原活性[8], SCHMITZ等[17]研究了两种用甲基取代C-2位酸性质子的改性咪唑类离子液体, 使用两种改性的离子液体作为电解质组分, 40℃下, 在Li||LFP电池前90个循环里比放电容量和库仑效率均优于未改性离子液体电池。
1.1.3 季铵盐类和季膦盐类
季铵盐类离子液体具有较高的电化学稳定性, 氧化电位高于5.0 V(vs. Li/Li+), 还原电位低于0 V(vs. Li/Li+), 不容易发生氧化还原反应。但季铵阳离子体积较大, 导致此类离子液体的黏度偏高, 离子电导率较低, SUN等[18]研究了一系列烷基季铵盐, 测得N-三乙基-N-正己基季铵双三氟甲磺酰亚胺盐(N2226-TFSI)的离子电导率最高, 但仅为6.7 × 10-4 S/cm。RAUBER等[19]研究了一系列三甲基季铵盐离子液体, 与N-三甲基-N-正戊基季铵三氟甲磺酰亚胺盐(N1115-TFSI)相比, N-三甲基-N-正丁基季铵三氟甲磺酰亚胺盐(N1114-TFSI)和N-三甲基-2-乙氧基季铵三氟甲磺酰亚胺盐(N111(2O2)-TFSI)的黏度分别从136.9 mPa∙ s降低至99.17 mPa∙ s和57.81 mPa∙ s, 室温离子电导率分别从1.35 × 10-3 S/cm升高至1.99 × 10-3 S/cm和2.90 × 10-3 S/cm。证明缩短侧链和引入适量醚基能够有效降低离子液体的黏度, 提高离子电导率。季膦盐类离子液体与季铵盐类离子液体结构类似, TSUNASHIMA等[20]发现取代基相同时, 季膦盐类离子液体相较于季胺盐类离子液体表现出更低的黏度和更高的离子电导率, 例如P-三乙基-P-正戊基季膦双三氟甲磺酰亚胺盐(P2225-TFSI)的黏度为88 mPa∙ s, 离子电导率为1.73 × 10-3 S/cm, 而N-三乙基-N-正戊基季铵双三氟甲磺酰亚胺盐(N2225-TFSI)的黏度和离子电导率分别为172 mPa∙ s和9.8 × 10-4 S/cm。
1.1.4 吡咯类和哌啶类
吡咯烷类和哌啶类离子液体可以看作是环状的季铵盐类离子液体, 前者为五元环, 后者为六元环。两者与季铵盐类离子液体类似, 都具有优异的电化学稳定性, 另外环状结构更接近于平面, 使得两种离子液体的黏度相对较低, 离子电导率较高, 在高温下更稳定[21]。由N-甲基-N-丙基吡咯烷鎓双三氟甲磺酰亚胺盐(Pyr13-TFSI)和双三氟甲磺酰亚胺锂(LiTFSI)组成的电解液热分解温度接近400℃, 氧化电位达到5.3 V(vs. Li/Li+), 在高温下具有良好的性能[22, 23, 24], 75℃时, Li||LFP电池在1 C和2 C的恒电流条件下分别具有150.9 mA∙ h/g和140.9 mA∙ h/g的放电容量。
以阴离子结构不同来划分, 离子液体可分为卤化盐类, 如Cl-、Br-、I-等; 非卤化盐类, 如PF6-、BF4-、TFSI-、FSI-等[25, 26]。而作为电解质常用的阴离子主要为非卤化盐类, 包括BF4- [27, 28]、FSI- [29, 30]、TFSI-[31]和PF6-[32]。其中含有BF4-和PF6-的离子液体在空气和水氛围下相对稳定, 但与路易斯酸反应强烈。而FSI-和TFSI-具有以下特点:首先, 这两种离子的电荷分布高度非定域, 减弱了离子液体中阴、阳离子之间的相互作用; 其次, 阴离子两端的-SO2CF3基团可以旋转, 使得结构具有一定的灵活性; 最后, 它们都具有较小的离子半径(TFSI-为0.379 nm, FSI-为0.264 nm)[8]。这些特点可以降低离子液体的黏度, 在锂离子电池中促进锂离子的转移, 提高离子电导率, 因此FSI-和TFSI-是离子液体中最常用的两种阴离子。
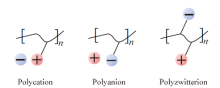
聚离子液体[poly(ionic liquid)s, PIL]是一类重复单元中包含离子液体单体的聚合物[33]。PIL可以由离子液体单体直接聚合或由离子液体和其他单体混合进行嵌段聚合来制备, 也可使用离子液体对已有聚合物进行改性/修饰得到PIL[34]。根据主链上离子所带电荷不同, 可分为聚阴离子液体、聚阳离子液体和聚两性离子液体(图2)。与离子液体相比, 聚离子液体继承了离子液体优异的热稳定性及电化学稳定性和不易燃等优点, 而且具有更高的可加工性、安全性和机械性能, 同时无漏液风险, 是开发新一代聚合物电解质的优秀原材料[35]。
锂离子电池的电解液通常由碳酸酯类有机溶剂[如碳酸乙烯酯(ethylene carbonate, EC)、碳酸丙烯酯(propylene carbonate, PC)、碳酸二甲酯(dimethyl carbonate, DMC)或碳酸二乙酯(diethyl carbonate, DEC)等]和锂盐组成, 这些有机溶剂具有高挥发性和易燃性, 是导致电池安全问题的主要原因。离子液体具有阻燃性和良好的热稳定性, 将其作为电解质的组分, 可以提高电池的安全性[9]。另外, 功能化的离子液体可以在石墨或锂金属负极形成固体电解质界面(solid electrolyte interface, SEI)膜, 抑制锂枝晶生长, 从而提高电池使用寿命和安全性[36, 37, 38, 39]。
离子液体可以直接作为电解液中的溶剂, 然而此类电解液的离子电导率受黏度影响很大, 而电解液的黏度与离子液体结构、温度和锂盐浓度有很大关系。
SANO等[40]使用N-甲基-N-丁基吡咯烷双三氟甲磺酰亚胺盐(C4mpyr-TFSI)作为电解液溶剂, 比较所配电解液离子电导率与黏度和温度的关系(表1), 可以看出随着温度升高, 电解液的黏度降低, 离子电导率增大, 并且发现C4mpyr-TFSI能够有效抑制锂枝晶在锂金属负极生成。
| 表1 质量比为10∶ 1的 (C4mpyr-TFSI)∶ LiTFSI电解质的电导率与温度和黏度关系[40] Table 1 Conductivity versus temperature and viscosity of C4mpyr-TFSI:LiTFSI (mass ratio of 10:1) electrolyte[40] |
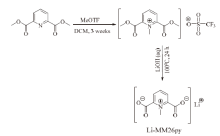
对离子液体结构进行优化设计可提高纯离子液体电解质的离子电导率, HOSSEINI-BAB-ANARI等[41]设计合成了1-甲基吡啶鎓2, 6-二羧酸锂(Li-MM26py)(图3), 其溶解在N-甲基-N-丁基吡咯烷鎓双三氟甲磺酰亚胺盐(Pyr14-TFSI)中得到混合阴离子电解液, 离子电导率在室温下可以达到3.2 × 10-3 S/cm。
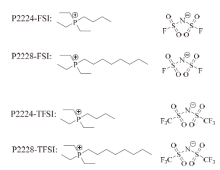
锂盐浓度的增加会增加电解质体系中锂离子的数量, 但高锂盐浓度会增大离子液体的黏度, 降低离子电导率。SÁ NCHEZ-RAMÍ REZ等[42]研究了四种季膦类离子液体(图4), 在25℃下, 向四种离子液体中分别加入1 mol/L LiTFSI后, 四种离子液体的黏度全部增大, 离子电导率全部减小。因此, 在纯离子液体基电解质中, 应在锂盐浓度和黏度之间寻求最佳配比, 以实现最优的电化学性能。
如前所述, 离子液体通常黏度较大, 离子电导率较低, 其作为纯电解质材料在锂电池中应用有一定的局限性。因此, 众多研究人员通过将离子液体和有机溶剂混合, 降低黏度, 提高离子电导率。这些引入离子液体的有机电解液还能提高电池的容量保持率, 改善电池的电化学性能。
陈真等[43]使用乙二醇二甲醚(ethylene glycol dimethyl ether, DME)作为1-乙基-3-甲基咪唑双三氟甲磺酰亚胺盐(EMI-TFSI)的共溶剂配制电解液。加入DME后, EMI-TFSI的黏度大幅下降, 离子电导率从5.93 × 10-3 S/cm提高到了1.42 × 10-2 S/cm。ZHANG等[44]合成了一种新型季铵类两性离子液体TL-TFSI, 有机离子结构上同时含有季铵阳离子和磺酸阴离子, 不含锂盐的TL-TFSI在常温下离子电导率为3.7 × 10-3S/cm, 将其加入1.9 mol/L LiTFSI/DOL + DME(体积比为1∶ 1), 得到的电解液不易燃(图5), 常温下离子电导率提高到4.1 × 10-3 S/cm。TL-TFSI的合成路线如图6a所示。
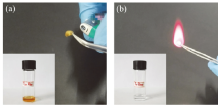 | 图5 脱脂棉浸入T70D30(a)和T0D100(b)电解液后的燃烧试验[44]Fig. 5 Lighted degreased cotton after dipping into the T70D30 electrolyte (a) or T0D100 electrolyte (b)[44] |
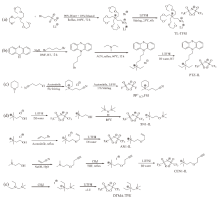 | 图6 离子液体的合成路线:两性离子液体TLTFSI(a)[44]、PTZ-IL(b)[46]、PP+1, CNFSI(c)[49]; (d)胆碱型离子液体SN1-IL、AN1-IL、CEN1-IL[50]; (e)DTMA-TFSI[51]Fig. 6 Synthesis routs of the ILs: zwitterionic ILs TLTFSI (a)[44], PTZ-IL (b)[46], PP+1, CNFSI (c)[49]; (d) functionalized choline ILs SN1-IL, AN1-IL and CEN1-IL[50]; (e) DTMA-TFSI[51] |
MA等[45]以Pyr13-TFSI、环丁砜(tetramethylene sulfone, SL)和碳酸甲乙酯(ethyl methyl carbonate, EMC)作为混合溶剂, 二氟草酸硼酸锂(lithium Difluoro(oxalato)borate, LiDFOB)为锂盐组成电解液, 在常温、0.5 C恒电流条件下100次循环后, Li||NCM811电池的容量保持率为97.6%。YOON等[46]利用吩噻嗪(phenothiazine, PTZ)合成了一种季铵盐类的离子液体PTZ-IL(图6b), 与三甘醇二甲醚(triethylene glycol dimethyl ether, TEGDME)和LiTFSI组成电解液。季铵结构的引入能够有效阻止PTZ与锂金属之间的反应, 在Li||Li对称电池中促进锂稳定地剥离/电镀; 另外, 与使用原始PTZ电解液相比, 使用PTZ-IL电解液的锂空气电池显示出更高的放电容量, 达到2 500 mA∙ h/g, 循环寿命延长了2倍。
SHOMURA等[47]发现将一系列吡啶类离子液体加入1 mol/L LiPF6/EC + DEC + 2, 2-二氟碳酸二乙酯(2, 2-difluoroethyl ethyl carbonate, FDEC)(体积比为28.5∶ 66.5∶ 5)电解液中, 可以在锂离子电池正极表面形成稳定的SEI膜, 提高锂离子电池的循环容量。LARHRIB等[48]通过向1 mol/L LiPF6/EC + EMC(质量比为1∶ 1)电解液中添加质量分数为30%的甲基三乙基膦双三氟甲烷磺酰亚胺盐(Bu3MeP-TFSI), 得到的电解液不易燃, 而且在60℃下, Bu3MeP-TFSI可以显著提高Li||NCA电池正极的容量(230 mA∙ h/g)和库仑效率(> 99%)。
ZHANG等[49]合成了一种新型离子液体N-丁腈-N-甲基哌啶鎓双氟磺酰亚胺盐(PP+1, CN-FSI)(图6c), 将其加入1 mol/L LiPF6/EC + DMC(质量比为1∶ 1)电解液中。在Li||LNMO电池中, 与使用原始电解液的电池相比, 添加质量分数为15% PP+1, CN-FSI的电池在0.2 C恒电流条件下50次循环后的容量保持率从82.8%提高到96.8%, 并且发现PP+1, CNFSI能够抑制电池过充电现象。
本课题组[50]使用三甲基硅基(SN1)、烯丙基(AN1)和氰乙基(CEN1)取代胆碱中的羟基合成了三种胆碱型离子液体(图6d)。对于纯的三种离子液体, AN1-IL具有最高的离子电导率, 常温下为4.29 × 10-3 S/cm。配制0.6 mol/L LiPF6+ 0.4 mol/L LiODFB/SN1-IL + DMC(体积比为1∶ 1)电解液, 在石墨||LiCoO2电池中显示出优异的循环性能, 在4.4 V的高电压下90次循环后, 仍具有152 mA∙ h/g的容量。
另外, 本课题组[51]设计合成了一种离子塑晶N, N, N, -二乙基甲基-N-[(三甲基硅基)甲基]双三氟甲磺酰亚胺盐(DTMA-TFSI)(图6e), DTMA-TFSI的熔点为54℃, 常温下为固体, 将其和PC混合, 以LiODFB为锂盐, 得到了一种固态的离子塑晶电解质。随着锂盐含量增加, DTMA-TFSI电解质的熔点逐渐降低, 当掺杂质量分数为30%的LiODFB时熔点降至43℃。通过优化各组分比例, 常温下离子电导率最高为1 × 10-4 S/cm。
离子液体可以作为增塑剂与聚合物[52, 53, 54]或无机材料[55, 56, 57, 58]复合制备准固态电解质, 此类电解质不仅具有离子液体的高安全性, 而且离子液体可以与其他组分共同形成特殊的离子通道, 有助于锂离子的传导, 通过各组分协同作用, 电解质能够表现出优异的综合性能。
MEGHNANI等[59]将1-丁基-3-甲基咪唑双三氟甲磺酰亚胺盐(C4MMIm-TFSI)混合PEO制备电解质, C4MMIm-TFSI的加入能够明显减少PEO中的结晶区(图7)。DING等[60]将氢化硼纳米片、PEO、EMIM-TFSI和LiTFSI混合, 得到电解质。在不加离子液体时, 电解质的离子电导率很低, 不能使电池正常工作。优化各组分比例, 常温下离子电导率最高为3.1 × 10-3 S/cm。
 | 图7 初始PEO(a)和PEO + 20%LiFSI + 20%IL(b)的SEM图像[59]Fig. 7 SEM images of pristine PEO (a) and PEO + 20%LiFSI + 20%IL (b)[59] |
SINGH等[61]利用Pyr13-FSI与聚偏二氟乙烯-六氟丙烯(PVDF-HFP)混合得到电解质, 30℃时, 离子电导率可达1.6 × 10-3 S/cm。LIN等[62]利用PVDF、N-甲氧基乙基-N-甲基吡咯烷鎓双三氟甲磺酰亚胺盐[Pyr1(2O1)-TFSI]和陶瓷电解质磷酸锗铝锂[Li1.5Al0.5Ge1.5(PO4)3, LAGP]混合, 得到的电解质在锂金属电池中能够显著抑制锂枝晶的生成。PAN等[63]使用N-甲基-N-丙基哌啶双三氟甲磺酰亚胺盐(PP13-TFSI)、PVDF-HFP、LiTFSI和TiO2, MgO, SiO2, ZrO2, CeO2, NiO, Bi2O3, Al2O3等氧化物制备了一系列复合电解质, 发现添加质量分数为5%的TiO2不仅可提高电解质的离子电导率(1.51 × 10-3 S/cm, 30℃), 还可改善电解质的机械性能。BARBOSA等[64]以斜方沸石(clinoptilolite, CPT)与PVDF-HFP和离子液体1-丁基-3-甲基咪唑硫氰酸盐(BMIM-SCN)组成一种不含锂盐的三元复合电解质, 室温下离子电导率达到1.9 × 10-4 S/cm。
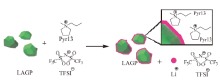
DING等[65]通过水热反应得到一种Na-X沸石, 锂化后得到Li-X沸石, 将Li-X沸石与EMIM-TFSI和LiTFSI混合, 压片得到固态电解质, 其30℃时离子电导率最高为1.2 × 10-4 S/cm。以此电解质组装的Li||LFP电池在60℃、0.5 C恒电流条件下, 850次循环后容量保持率为96%。PAOLELLA等[66]利用陶瓷电解质LAGP和Pyr13-TFSI与LiTFSI组成电解质, LAGP和Pyr13-TFSI之间能够发生离子交换反应, 形成LiTFSI(图8), 有助于提高离子电导率, 优化后电解质常温下的离子电导率最高为1.5 × 10-4 S/cm。
研究人员发现MOF中的金属原子与TFSI阴离子之间具有强相互作用, 有助于离子液体和LiTFSI的解离, 因此, 将离子液体封装在MOF材料中可以获得较高的离子电导率。ZETTL等[67]报道了一种MIL-121 MOF材料, 向其中加入 EMIM-TFSI和LiTFSI, 离子电导率最高可以达到5 × 10-4S/cm。
聚离子液体失去了离子液体的流动性, 进一步克服了电解液漏液的风险。相对于传统的聚合物电解质基体(PEO、PVDF、PAN等), 聚离子液体电解质一般具有更高的离子电导率和良好的电化学稳定性。同时这类电解质一般具有良好的热稳定性和阻燃性, 热分解温度通常在300℃以上, 增强了电池的安全性。
聚离子液体和锂盐复合, 不添加溶剂时, 得到聚离子液体电解质。
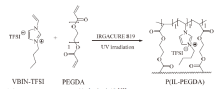
ZHANG等[68]将1-乙烯基-3-丁基咪唑双三氟甲磺酰亚胺盐(VBIm-TFSI)和PEGDA原位聚合, 加入LiTFSI, 得到一种固态电解质P(IL-PEGDA)(图9), 其热分解温度为325℃。在室温和0.2 C恒电流条件下, P(IL-PEGDA)在Li||LFP电池中能够有效抑制锂枝晶的生长, 并且具有140 mA∙ h/g的可逆比容量和接近100%的库伦效率。通过优化各组分的比例, 30℃时, P(IL-PEGDA) 的离子电导率最高为1.4 × 10-4 S/cm。
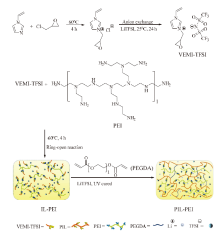
LIANG等[69]合成一种新型离子液体1-乙烯基-3-环氧丙基咪唑双三氟甲基磺酰亚胺盐(VEMI-TFSI), 并将其接枝到聚乙烯亚胺(polyethylenimine, PEI)的胺基上, 再用聚乙二醇二丙烯酸酯(PEGDA)作为交联剂, 并加入LiTFSI, 得到固态电解质PIL-PEI(图10)。与商用隔膜Celgard 2400相比, PIL-PEI的热分解温度为360℃, 并且具有阻燃性。优化后PIL-PEI室温下的离子电导率最高为1.03 × 10-3 S/cm。
由于PIL和离子液体之间具有较强的化学亲和力, 离子液体可以被很好地封装在PIL中, 因此常使用离子液体和PIL复合制备准固态电解质[70, 71, 72]。
SHA等[73]将1-乙氧基甲基-3-乙烯基咪唑双三氟甲磺酰亚胺盐(Vmim1O2-TFSI)、PVDF-HFP、PEGDA和LiTFSI原位聚合, 以EMIM-TFSI作为增塑剂, 得到一种半互穿结构的电解质。该电解质膜具有良好的机械性能, 25℃下离子电导率最高为1.06 × 10-3 S/cm。
值得一提的是, 离子塑晶也可作为固态增塑剂, 与聚离子液体复合制备电解质。YANG等[74]合成了一种新型有机离子塑晶三乙基甲基铵双氟磺酰亚胺盐(N1222-FSI), 并将其引入聚(二烯丙基二甲基铵)双三氟甲磺酰亚胺[P(DADMA-TFSI)]中, 制备了一系列N1222-FSI-PIL-LiTFSI电解质, 其室温下离子电导率最高为2 × 10-4 S/cm。
某些无机物与聚离子液体材料复合, 通过组分协同作用可提高材料的离子电导率和机械性能, 同时电池的容量保持率和使用寿命也可以得到改善。
TSENG等[75]通过原位聚合将TiO2纳米粒子混入离子液体聚合物基体中, 其中添加质量分数为0.5% 的TiO2纳米粒子的样品在室温下的离子电导率最高, 为1.97 × 10-4 S/cm, 高于不含TiO2的样品(1.51 × 10-4 S/cm)。以此为电解质组装的Li||LFP电池在25℃、0.2 C条件下的比放电容量为149 mA∙ h/g, 140次循环后, 容量保持率为90%。
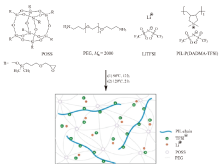
多面体低聚倍半硅氧烷(polyhedral oligomeric silsesquioxane, POSS)是一类有机/无机纳米杂化分子[76], 可以和聚离子液体混合制备复合电解质。LI等[77]在POSS-聚乙二醇基电解质体系中掺入P(DADMA-TFSI), 得到一种半互穿的复合电解质(PIL-IPN)(图11), 其常温下的离子电导率最高为1.86 × 10-5 S/cm。以PIL-IPN组装的Li|| LFP电池在90℃、0.5 C恒流充放电条件下, 电池的放电容量约为150 mA∙ h/g, 50次充放电循环后, 库伦效率超过99%。YANG等[78]使用一种简单的多加成法, 由共价键连接POSS、2, 2-二(1-亚甲基-3-丁基-咪唑鎓)-1, 3-丙二醇(ILs)、聚乙二醇(polyethylene glycol, PEG)和脲基嘧啶酮(UPy), 制备了一种新型的复合电解质(PIEU), 其室温下离子电导率最高为3.44 × 10-5 S/cm。PIEU存在多个具有解离和复合能力的动态氢键, 使得电解质具有一定的自修复能力, 同时, 咪唑阳离子与TFSI-之间的离子相互作用能协助愈合。
综述了近年来不同种类(聚)离子液体电解质的设计合成及其在锂离子电池中的最新应用进展, 归纳总结了(聚)离子液体电解质的优势:在室温下实现高离子电导率对于离子液体电解质应用非常重要, 离子液体可以通过与有机电解液复合降低黏度, 从而提高离子电导率; 离子液体也可与无机或高分子材料复合制备高离子电导率的准固态电解质, 并改善固态电解质的加工性能和电化学性能; 功能化的离子液体具有阻燃性, 并且能在石墨或锂金属负极表面形成特殊组分的SEI膜, 抑制锂枝晶的生长, 提高电池的容量保持率和安全性; 聚离子液体继承了离子液体良好的热稳定性和阻燃性的优点, 还兼具了聚合物固态电解质在电池制作时不漏液和易于加工等优势, 是一种具有应用前景的固态电解质材料。
与普通有机电解液相比, 离子液体电解质的最大的优势是安全性, 在锂离子电池中的实际应用有光明前景, 但仍面临着一些困难和挑战:(1)在不同类型的离子液体中, 咪唑类离子液体的黏度最小, 离子电导率最高, 最接近商用电解液, 但是其电化学窗口较窄, 会导致电池寿命缩短, 增加C-2位取代基可以改善其电化学稳定性, 但会导致离子电导率下降, 因此需要在两者之间寻求最优解。(2)在离子液体的合成过程中, 一般先用卤代化合物与仲胺、咪唑等发生亲核取代, 得到以卤素为阴离子的离子液体, 然后进行离子交换。因此最终得到的离子液体会混有少量卤素离子, 易腐蚀电极, 造成短路。可以在合成时选择不含卤素的化合物, 如三氟甲磺酸酯等, 获得高纯度无卤素的离子液体材料。(3)相对于碳酸酯类电解液, 离子液体的生产成本很高, 制约了离子液体的实际应用, 可以通过扩大生产规模、探索新的合成方法来降低成本。
随着人们对储能器件在安全性、能量密度和使用寿命等方面的要求越来越高, 今后研究人员需要不断深入对离子液体与聚离子液体的性质理论研究, 设计合成新型离子液体材料, 以期获得经济与实用兼具的离子液体电解质材料。
| [1] |
|
| [2] |
|
| [3] |
|
| [4] |
|
| [5] |
|
| [6] |
|
| [7] |
|
| [8] |
|
| [9] |
|
| [10] |
|
| [11] |
|
| [12] |
|
| [13] |
|
| [14] |
|
| [15] |
|
| [16] |
|
| [17] |
|
| [18] |
|
| [19] |
|
| [20] |
|
| [21] |
|
| [22] |
|
| [23] |
|
| [24] |
|
| [25] |
|
| [26] |
|
| [27] |
|
| [28] |
|
| [29] |
|
| [30] |
|
| [31] |
|
| [32] |
|
| [33] |
|
| [34] |
|
| [35] |
|
| [36] |
|
| [37] |
|
| [38] |
|
| [39] |
|
| [40] |
|
| [41] |
|
| [42] |
|
| [43] |
|
| [44] |
|
| [45] |
|
| [46] |
|
| [47] |
|
| [48] |
|
| [49] |
|
| [50] |
|
| [51] |
|
| [52] |
|
| [53] |
|
| [54] |
|
| [55] |
|
| [56] |
|
| [57] |
|
| [58] |
|
| [59] |
|
| [60] |
|
| [61] |
|
| [62] |
|
| [63] |
|
| [64] |
|
| [65] |
|
| [66] |
|
| [67] |
|
| [68] |
|
| [69] |
|
| [70] |
|
| [71] |
|
| [72] |
|
| [73] |
|
| [74] |
|
| [75] |
|
| [76] |
|
| [77] |
|
| [78] |
|