0 引言
1 材料与方法
1.1 原料与试剂
1.2 实验方法
1.3 分析表征方法
2 结果与讨论
2.1 碱催化甘油水溶液预处理甘蔗渣的条件
Table 1 Effect of pretreatment temperature on the deconstruction of lignocellulosic biomass表1 预处理温度对生物质组分拆解的影响 |
| 预处理温度/℃ | 回收率/% | 组分含量/% | 组分保留率/% | 木质素脱除率/% | ||||
|---|---|---|---|---|---|---|---|---|
| 纤维素 | 半纤维素 | 木质素 | 纤维素 | 半纤维素 | ||||
| 120 | 85.60 | 44.17 | 24.27 | 18.22 | 96.80 | 94.39 | 38.09 | |
| 140 | 75.40 | 50.44 | 27.79 | 12.72 | 97.37 | 95.20 | 61.93 | |
| 160 | 71.70 | 50.57 | 26.69 | 13.10 | 92.83 | 86.95 | 62.71 | |
| 180 | 69.80 | 51.37 | 26.84 | 11.75 | 91.80 | 85.12 | 67.44 | |
| 200 | 68.90 | 50.35 | 25.60 | 9.90 | 88.82 | 80.14 | 72.92 | |
注:NaOH浓度为5.0%,预处理时间为30 min,甘油浓度为80%。 |
Table 2 Effect of alkali addition on the deconstruction of lignocellulosic biomass表2 加碱量对生物质组分拆解的影响 |
| NaOH浓度/% | 回收率/% | 组分含量/% | 组分保留率/% | 木质素脱除率/% | ||||
|---|---|---|---|---|---|---|---|---|
| 纤维素 | 半纤维素 | 木质素 | 纤维素 | 半纤维素 | ||||
| 1.0 | 80.00 | 45.88 | 25.01 | 19.77 | 93.97 | 90.90 | 37.22 | |
| 3.0 | 74.30 | 49.32 | 26.53 | 12.23 | 93.82 | 89.56 | 63.92 | |
| 5.0 | 69.80 | 51.37 | 26.84 | 11.75 | 91.80 | 85.12 | 67.44 | |
| 7.0 | 67.70 | 52.96 | 26.82 | 8.23 | 91.79 | 82.49 | 77.88 | |
| 9.0 | 65.50 | 54.30 | 27.73 | 6.60 | 91.06 | 82.52 | 82.84 | |
注:预处理温度为180β℃,预处理时间为30 min,甘油浓度为80%。 |
Table 3 Effect of pretreatment time on the deconstruction of lignocellulosic biomass表3 预处理时间对生物质组分拆解的影响 |
| 预处理时间/min | 回收率/% | 组分含量/% | 组分保留率/% | 木质素脱除率/% | ||||
|---|---|---|---|---|---|---|---|---|
| 纤维素 | 半纤维素 | 木质素 | 纤维素 | 半纤维素 | ||||
| 15 | 68.13 | 52.27 | 26.81 | 8.68 | 91.17 | 82.99 | 76.52 | |
| 30 | 67.70 | 52.96 | 26.82 | 8.23 | 91.79 | 82.49 | 77.88 | |
| 45 | 67.00 | 54.24 | 27.40 | 8.10 | 93.04 | 83.41 | 78.46 | |
| 60 | 66.00 | 54.14 | 27.59 | 8.16 | 91.48 | 82.73 | 78.62 | |
| 90 | 65.00 | 55.22 | 27.00 | 7.81 | 91.90 | 79.74 | 79.85 | |
注:预处理温度为180β℃,NaOH浓度为7.0%,甘油浓度为80%。 |
Table 4 Effect of glycerol percentage on the deconstruction of lignocellulosic biomass表4 甘油浓度对生物质组分拆解的影响 |
| 甘油浓度/% | 回收率/% | 组分含量/% | 组分保留率/% | 木质素脱除率/% | ||||
|---|---|---|---|---|---|---|---|---|
| 纤维素 | 半纤维素 | 木质素 | 纤维素 | 半纤维素 | ||||
| 30 | 64.60 | 52.99 | 27.13 | 10.35 | 87.64 | 79.63 | 73.46 | |
| 45 | 65.10 | 53.61 | 27.34 | 9.35 | 89.35 | 80.86 | 75.84 | |
| 60 | 66.00 | 53.42 | 27.38 | 8.70 | 90.26 | 82.10 | 77.21 | |
| 75 | 66.20 | 53.48 | 27.36 | 8.43 | 90.64 | 82.29 | 77.85 | |
| 80 | 67.00 | 54.24 | 27.40 | 8.10 | 93.04 | 83.41 | 78.46 | |
| 90 | 67.50 | 54.70 | 27.51 | 7.80 | 94.53 | 84.37 | 79.10 | |
| 100 | 67.70 | 54.92 | 27.59 | 7.62 | 95.19 | 84.86 | 79.52 | |
注:预处理温度为180β℃,NaOH浓度为7.0%,预处理时间为45 min。 |
2.2 预处理底物的可酶解性
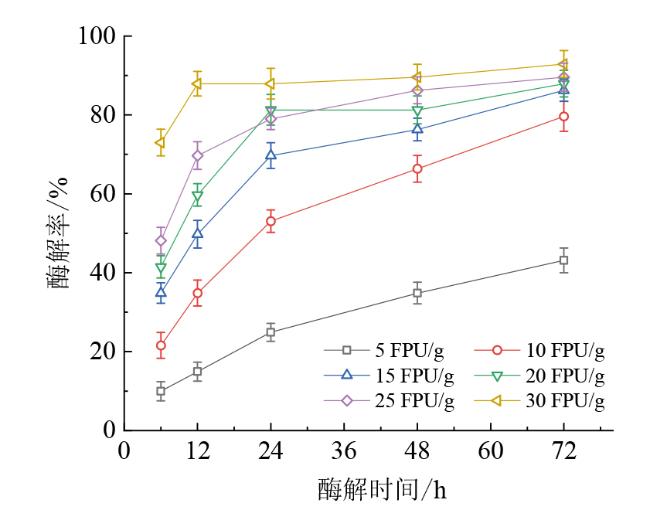
Fig. 1 Enzymatic hydrolysis of the pretreated substrates under different enzyme dosages图1 不同酶载量下预处理底物的酶解情况 |
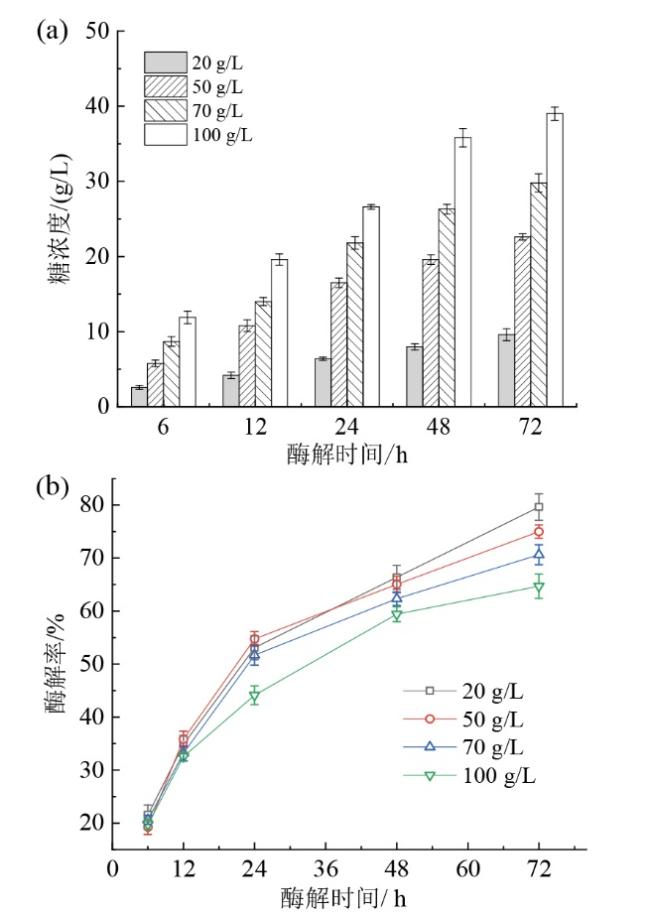
Fig. 2 Enzymatic hydrolysis of the pretreated substrates under different solid loadings: (a) sugar titer; (b) hydrolysis yield图2 预处理底物在不同底物浓度下的酶解情况:(a)糖浓度;(b)酶解率 |
2.3 底物预处理前后的结构解析
Fig. 3 Scanning electron microscope diagram of sugarcane bagasse raw material (a) and pretreated sample (b)图3 甘蔗渣原料(a)及预处理样品(b)扫描电镜图 |
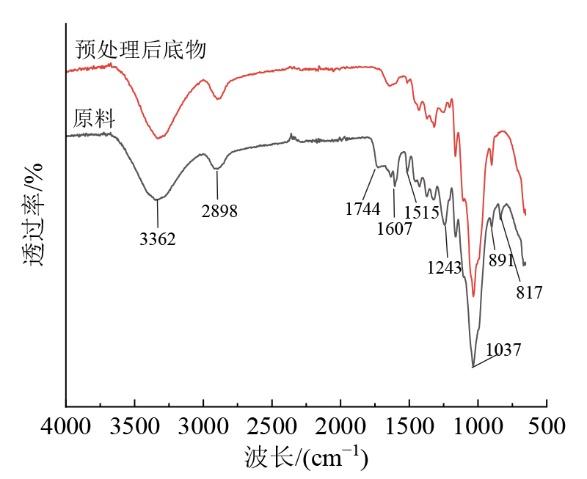
Fig. 4 Changes in functional groups of biomass fractions before and after pretreatment图4 预处理前后生物质组分的官能团变化 |
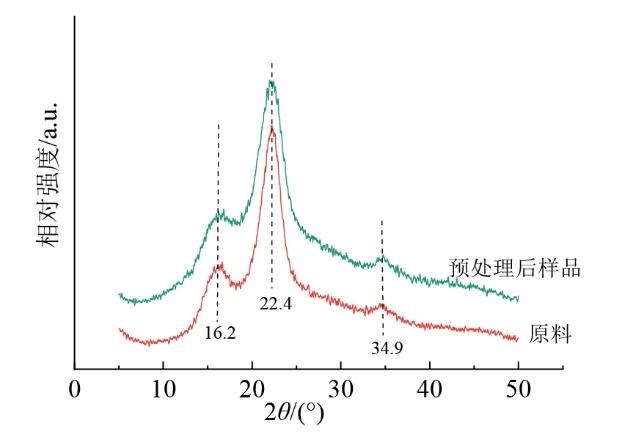
Fig. 5 X-ray diffraction analysis of different samples图5 不同样品的X射线衍射分析 |