0 引言
1 生物质含氧有机废液水相重整
Table 1 Comparison of hydrogen production methods from oxygenated organic waste liquid表1 含氧有机废液制氢方式对比 |
| 制氢方式 | 反应过程 | 优点 | 缺点 |
|---|---|---|---|
| 光催化析氢[3,4,5] | 光催化材料吸收光能,催化转化原料中有机物 | 环境友好 | 催化剂选择范围窄、催化效率低、成本高 |
| 微生物催化产氢[6,7] | 微生物菌群或某种细菌在适宜条件下,催化分解废液 | 成本低、环境友好、能量输入低 | 效率低、催化环境要求苛刻、产量低 |
| 电解废液制氢[8,9] | 在有水的电解池中施加电压,将水直接分解为氢气和氧气 | 无需催化剂、氢气纯度高 | 耗电量大、成本高、电极易腐蚀 |
| 超临界水制氢[10,11] | 利用超临界状态的较高溶解度和反应活性水平,削弱氢键键能,增强传质和传热,在较短时间内实现氢气生产和废液处理 | 反应速率快 | 成本高、操作困难、条件苛刻、催化剂选择范围窄 |
| 蒸汽重整制氢[12,13,14] | 预处理成低盐废液后,在高温高压条件下,催化废液中有机物与高温水蒸气反应 | 反应速率快、高效能、催化剂选择范围广、环保 | 气化耗能高、副反应多、反应条件苛刻、原料处理过程繁琐 |
| 水相重整制氢[15,16,17] | 在温和条件下催化废液中有机物和水反应 | 低能耗、高效、可原位制氢,副产物少、环境友好、成本低 | 发展缓慢 |
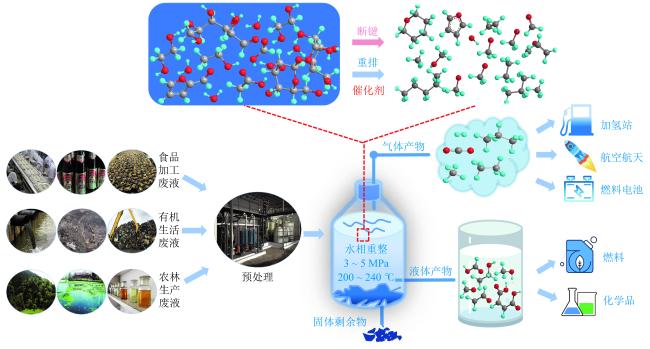
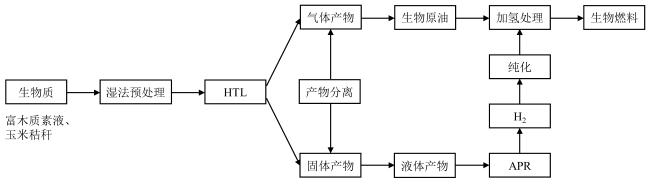
Fig. 1 Conceptual diagram of value-added chemicals production through aqueous phase reforming of biomass oxygenated organic waste liquid图1 生物质含氧有机废液水相重整生产增值化学品示意图 |
Table 2 Reaction equations related to the aqueous phase reforming of oxygenated organic waste liquid表2 含氧有机废液水相重整相关反应式 |
| 反应类型 | 反应名称 | 反应方程式 | 反应能垒 | 编号 |
|---|---|---|---|---|
| 水相重整反应 | 重整反应 | ${{\text{C}}_{n}}{{\text{H}}_{2n+2}}{{\text{O}}_{n}}\to n\text{CO}+\left( n+1 \right){{\text{H}}_{2}}$ | ΔH > 0 | (1) |
| 水气变换 | $\text{CO}+{{\text{H}}_{2}}\text{O}\to \text{C}{{\text{O}}_{2}}+{{\text{H}}_{2}}$ | ΔH298K = -41 kJ/mol | (2) | |
| 总反应式 | ${{\text{C}}_{n}}{{\text{H}}_{2n+2}}{{\text{O}}_{n}}+n{{\text{H}}_{\text{2}}}\text{O}\to n\text{C}{{\text{O}}_{2}}+\left( 2n+1 \right){{\text{H}}_{2}}$ | ΔH > 0 | (3) | |
| 水相重整副反应 | 烃类重整 | ${{\text{C}}_{n}}{{\text{H}}_{m}}+n{{\text{H}}_{\text{2}}}\text{O}\to n\text{CO}+\left( n+0.5m \right){{\text{H}}_{2}}$ | — | (4) |
| 费托反应 | $n\text{CO}+2n{{\text{H}}_{2}}\to {{\text{C}}_{n}}{{\text{H}}_{2n}}+n{{\text{H}}_{\text{2}}}\text{O}$ | ΔH ˃ 0 | (5) | |
| 甲烷化 | $\text{CO}+3{{\text{H}}_{2}}\to \text{C}{{\text{H}}_{4}}+{{\text{H}}_{\text{2}}}\text{O}$ | ∆H298K = 206 kJ/mol | (6) | |
| $\begin{matrix} \text{C}{{\text{O}}_{2}}+4{{\text{H}}_{2}}\to \text{C}{{\text{H}}_{4}}+2{{\text{H}}_{\text{2}}}\text{O} \\ \end{matrix}$ | ∆H298K = 165 kJ/mol | (7) | ||
| 甲烷重整 | $\text{C}{{\text{H}}_{4}}+{{\text{H}}_{\text{2}}}\text{O}\to \text{CO}+\text{3}{{\text{H}}_{\text{2}}}$ | ∆H298K = 206 kJ/mol | (8) | |
| $\text{C}{{\text{H}}_{4}}+2{{\text{H}}_{\text{2}}}\text{O}\to \text{C}{{\text{O}}_{2}}+4{{\text{H}}_{\text{2}}}$ | ∆H298K = 165 kJ/mol | (9) | ||
| 逆水气变换 | $\text{C}{{\text{O}}_{\text{2}}}+{{\text{H}}_{2}}\to \text{CO}+{{\text{H}}_{\text{2}}}\text{O}$ | ΔH ˃ 0 | (10) | |
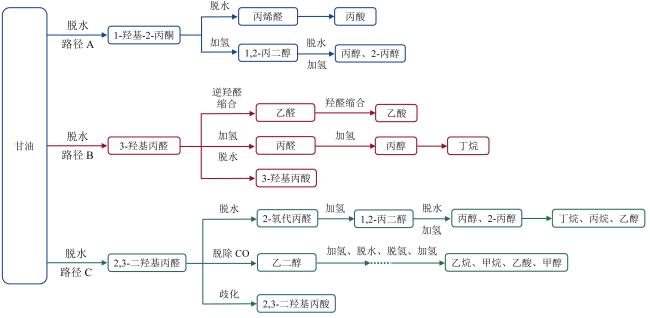
| 典型废液水相重整反应 | 葡萄糖脱水[19] | ${{\text{C}}_{\text{6}}}{{\text{H}}_{\text{12}}}{{\text{O}}_{\text{6}}}\xrightarrow{-3{{\text{H}}_{\text{2}}}\text{O}}{{\text{C}}_{\text{6}}}{{\text{H}}_{\text{6}}}{{\text{O}}_{\text{3}}}\xrightarrow{+2{{\text{H}}_{\text{2}}}\text{O}}{{\text{C}}_{\text{5}}}{{\text{H}}_{\text{8}}}{{\text{O}}_{\text{3}}}+\text{C}{{\text{H}}_{\text{2}}}{{\text{O}}_{\text{2}}}\xrightarrow{}\text{C}{{\text{O}}_{2}}+{{\text{H}}_{2}}$ | — | (11) |
| 丙氨酸水解[19] | $\mathrm{C}_3\mathrm{H}_7\mathrm{NO}_2\xrightarrow{\text{脱氨}}\mathrm{C}_3\mathrm{H}_6\mathrm{O}_3\xrightarrow{}\mathrm{C}_2\mathrm{H}_4\mathrm{O}+\left(\mathrm{CO}_2+\mathrm{H}_2\right)/\left(\mathrm{CO}+\mathrm{H}_2\mathrm{O}\right)$ | — | (12) | |
| 甘氨酸水解[19] | $\mathrm{C}_2\mathrm{H}_5\mathrm{NO}_2\xrightarrow{\text{脱氨}}\mathrm{C}_2\mathrm{H}_4\mathrm{O}_3\xrightarrow{}\mathrm{CH}_2\mathrm{O}_2+\left(\mathrm{CO}_2+\mathrm{H}_2\right)/\left(\mathrm{CO}+\mathrm{H}_2\mathrm{O}\right)$ | — | (13) | |
| 酒糟水相重整[16] | ${{\text{C}}_{\text{1127}\text{.95}}}{{\text{H}}_{\text{1272}\text{.58}}}{{\text{O}}_{\text{89}\text{.81}}}{{\text{N}}_{137.16}}+1512.305{{\text{H}}_{\text{2}}}\text{O}\to 1127.95\text{C}{{\text{O}}_{2}}+2148.595{{\text{H}}_{2}}+68.58{{\text{N}}_{2}}$ | — | (14) | |
| 海藻酸盐水相重整[29] | ${{\text{C}}_{\text{6}}}{{\text{H}}_{\text{9}}}{{\text{O}}_{\text{7}}}+5{{\text{H}}_{\text{2}}}\text{O}\to 6\text{C}{{\text{O}}_{2}}+9.5{{\text{H}}_{2}}$ | — | (15) | |
| 麦芽糖预加氢制麦芽糖醇[30] | ${{\text{C}}_{\text{12}}}{{\text{H}}_{\text{22}}}{{\text{O}}_{11}}+{{\text{H}}_{2}}\to {{\text{C}}_{\text{12}}}{{\text{H}}_{\text{24}}}{{\text{O}}_{\text{11}}}$ | — | (16) | |
| 麦芽糖水相重整[30] | ${{\text{C}}_{\text{12}}}{{\text{H}}_{\text{22}}}{{\text{O}}_{11}}+13{{\text{H}}_{\text{2}}}\text{O}\to 12\text{C}{{\text{O}}_{2}}+24{{\text{H}}_{\text{2}}}$ | — | (17) | |
| 麦芽糖醇水相重整[30] | ${{\text{C}}_{\text{12}}}{{\text{H}}_{\text{24}}}{{\text{O}}_{11}}+13{{\text{H}}_{\text{2}}}\text{O}\to 12\text{C}{{\text{O}}_{2}}+25{{\text{H}}_{2}}$ | — | (18) |
Table 3 Parameters for aqueous phase reforming of biomass oxygenated organic waste liquid表3 含氧有机废液水相重整原料参数 |
| 废水来源 | 初始TOC/(mg/L) | 初始COD/(mg/L) | 初始原料 | 参考文献 |
|---|---|---|---|---|
| 生活污水 | — | — | 复合浓度:淀粉230 mL/L、葡萄糖70 mL/L、肉蛋白胨420 mL/L、葵花籽油0.1 mL/L | [40] |
| 微藻和污泥 | — | — | 甘油、葡萄糖、丙氨酸和腐植酸 | [41] |
| 合成污水 | 约220 | 约1.3 | 水、蛋白质、碳水化合物、脂类和矿物盐 | [38] |
| 化妆品污水处理厂污泥废液的低浓度溶液 | 27 700 | 79 600 | 对氨基苯甲酸、苯并咪唑、苯并三唑衍生物肌酸等 | [2] |
| 酒糟处理废水 | 19 815 ± 77.78 | 63 600 ± 2 262.74 | 酒糟中温厌氧消化(发酵时间40天,发酵温度30β℃)得到 | [16] |
| 稻壳热解生物油低沸馏分 | — | — | 5.85%乙醇、9.33%醋酸甲酯、10.81%丙酮、31.64%醋酸、8.4%糠醛、5.16% 2-甲氧基苯酚 | [20] |
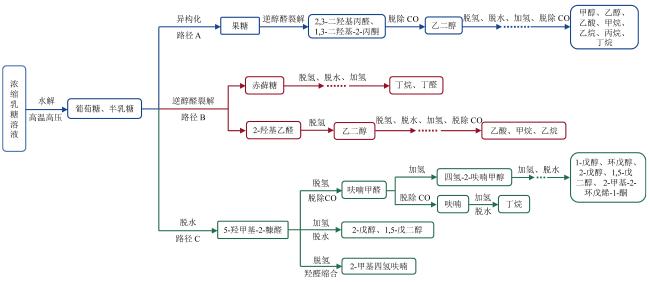
| 桦木水解物 | — | — | 甘露糖/半乳糖、葡萄糖、阿拉伯糖、二糖和三糖、甲酸、木糖、乙酸、糠醛和羟甲基糠醛 | [42] |
| 松木水解物 | — | — | 甘露糖/半乳糖、葡萄糖、阿拉伯糖、二糖和三糖以及甲酸 | [42] |
| 商用淀粉废水 | 4 014 ± 352 | 10 143 ± 331 | (9 908 ± 152) mg/L可溶性淀粉;乙酸、甲酸、丙二酸、草酸和富马酸的浓度非常低,约占初始TOC的0.3% | [17] |
| 合成啤酒废水 | 1 871 ± 79 | 5 846 ± 331 | 麦芽提取物(1 g/L)、酵母提取物(0.5 g/L)、蛋白胨(0.15 g/L)、 麦芽糖(0.86 g/L)、硫酸铵(1 g/L)、乙醇(2.8 mL/L) | [43] |
| 果汁废水 | 2 317 | 5 925 | 水合葡萄糖和果糖(共计约80%) | [44] |
| 奶酪乳清原料 | — | 50 000 ~ 102 000 | 4.5% ~ 6%乳糖、0.6% ~ 1.1%蛋白质、0.8% ~ 1%矿物质、0.05% ~ 0.9%乳酸、0.06% ~ 0.5%脂肪和93% ~ 94%水 | [18] |
| 金枪鱼烹饪废水 | 1 895 ± 258 | 4 996 ± 501 | 氯化物 (3 815 ± 219) mg/L、醋酸盐 (1 895 ± 321) mg/L、甲酸盐 (10 ± 9) mg/L、磷酸盐 (523 ± 22) mg/L、硫酸盐(16 ± 14) mg/L | [19] |
注:总有机碳(total organic carbon, TOC)指在液体中测量的所有有机碳的总量,包括溶解态和悬浮态的有机化合物;化学需氧量(chemical oxygen demand, COD)指氧化剂在特定条件下氧化有机物所需的氧化剂量;各物质的百分含量均指质量百分数。 |
2 有机生活废液水相重整
2.1 日常生活排放废液
2.2 污水污泥排放废液
Table 4 Organic living waste liquid aqueous phase reforming reaction表4 有机生活废液水相重整反应 |
| 反应底物 | 反应条件 | Rtoc(Rcod) | Si | 液相产物 | 参考文献 |
|---|---|---|---|---|---|
| 合成污水 | 0.3 g 3% Pt/ENSACO,220β℃,2.4 ~ 2.6 MPa,反应时间4 h,500 r/min,15 mL原料,pH = 8.6 | Rtoc = (55.3 ± 1.9)% | ${{S}_{{{\text{H}}_{\text{2}}}}}=(4.7\pm 0.3)\%$$~{{S}_{\text{C}{{\text{O}}_{\text{2}}}}}=(80.5\pm 1.0)\%$ $~{{S}_{\text{C}{{\text{H}}_{\text{4}}}}}=(9.4\pm 0.9)\%$ $~{{S}_{{{\text{C}}_{\text{2}}}{{\text{H}}_{\text{6}}}}}=(4.0\pm 0.2)\%$ $~{{S}_{{{\text{C}}_{\text{3}}}{{\text{H}}_{\text{8}}}}}=(1.4\pm 0.1)\%$ | — | [38] |
| 微藻和活性污泥模型化合物 | Pt/Al2O3-CeO2,245β℃,3.5 MPa,反应时间3 h,50 mL原料 | — | $~{{S}_{{{\text{H}}_{\text{2}}}}}=8.7%\tilde{\ }10.9\%$ | — | [41] |
| 化妆品污水处理厂污泥废液的低浓度溶液 | 0.4 g Pt/CBe,220β℃,2.5 ~ 2.9 MPa,反应时间4 h,500 r/min,20 mL原料,pH = 5 | Rtoc = 0.48% Rcod = 0.37% | $~{{S}_{{{\text{H}}_{\text{2}}}}}=0.31\%$ $~{{S}_{\text{C}{{\text{O}}_{\text{2}}}}}=0.58\%$ $~{{S}_{\text{C}{{\text{H}}_{\text{4}}}}}=9\%$ | 有机酸:醋酸、甲酸、丙二酸、赤霉酸、马来酸; 其他化合物:视黄醛、丁酮、加洛内酯、吡啶、芳香族化合物、胺、氯化物、卤代化合物 | [2] |
| 生活垃圾水热液化废水(光催化) | Fe/TiO2,反应时间3 h,20 mL原料 | — | $~{{S}_{{{\text{H}}_{\text{2}}}}}=27%\tilde{\ }37\%$ $~{{S}_{\text{C}{{\text{O}}_{\text{2}}}}}=17%\tilde{\ }24\%$ $~{{S}_{\text{CO}}}=17%\tilde{\ }24\%$ $~{{S}_{\text{C}{{\text{H}}_{\text{4}}}}}=23%\tilde{\ }27\%$ | 丙酸80 ~ 1 082 g/mL、甲酸300 ~ 675 g/mL、乙酸90 ~ 240 g/mL | [45] |
| 含微量化学污染物的合成污水 | 0.4 g Pt/ENSACO,220β℃,2.4 ~ 2.6 MPa,反应时间4 h,500 r/min,15 mL原料 | — | ${{S}_{{{\text{H}}_{\text{2}}}}}=(19.2\pm 0.7)\%$ $~{{S}_{\text{C}{{\text{O}}_{\text{2}}}}}=(63.8\pm 0.6)\%$ $~{{S}_{\text{C}{{\text{H}}_{\text{4}}}}}=(11.7\pm 0.6)\%$ $~{{S}_{{{\text{C}}_{\text{2}}}{{\text{H}}_{\text{6}}}}}=(3.9\pm 0.3)\%$ $~{{S}_{{{\text{C}}_{\text{3}}}{{\text{H}}_{\text{8}}}}}=(1.4\pm 0.2)\%$ | — | [38] |
注:Rtoc为总有机碳去除率,%;Rcod为化学需氧量去除率,%;Si为气体产物i的选择性,%。 |
2.3 垃圾处理排放废液
2.4 微量化学污染排放废液
3 农林生产废液水相重整
3.1 酒糟生产废液
Table 5 Aqueous phase reforming reaction for agricultural waste liquid表5 农业废液水相重整反应 |
| 反应底物 | 反应条件 | Si(产量) | 液相产物 | 参考文献 |
|---|---|---|---|---|
| DGBW | 1 g α-MNOV,225β℃, 3 MPa,反应时间30 h,1 000 r/min,50 mL原料 | 产量H2 = 245.60 mL,N2 = 308.67 mL | 酸类72.92%,醇类11.76%,乙醚5.78%,氮化物44.50%,芳香族4.24%,酰胺7.85% | [16] |
| 1 g Ni/α-MNOV,225β℃,3 MPa,反应时间30 h,1 000 r/min,50 mL原料 | 产量H2 = 191.67 mL,N2 = 230.17 mL | 酸类51.14%,醇类4.77%,乙醚22.85%,氮化物59.52%,芳香族5.48%,酰胺12.18% | ||
| 酒糟沼液 | 1 g 600β℃-α-MoO3纳米片,225β℃,3 MPa,反应时间0.5 h,200 r/min,50 mL原料 | 产量H2 = 245.60 mL,N2 = 308.67 mL | 羧酸10.48%,乙醚0.79%,氮化物90.76%,芳香族29.08%,酰胺58.93% | [49] |
| 1%海藻酸盐 | 0.8 g Pt/C,225β℃,3 MPa,反应时间6 h,500 r/min,100 mL原料,pH = 12 | $~{{S}_{{{\text{C}}_{\text{3}}}{{\text{H}}_{\text{8}}}}}=0.40%{{S}_{{{\text{H}}_{\text{2}}}}}=46.80\%$ $~{{S}_{\text{C}{{\text{O}}_{\text{2}}}}}=41.70%{{S}_{\text{C}{{\text{H}}_{\text{4}}}}}=5.90\%$ $~{{S}_{{{\text{C}}_{\text{2}}}{{\text{H}}_{\text{6}}}}}=1.90%{{S}_{{{\text{C}}_{\text{3}}}{{\text{H}}_{\text{8}}}}}=0.40\%$ | 乙酸、丙酸、琥珀酸、马来酸 | [29] |
| 生物油低沸馏分 | 0.5 g 2% Pt/Al2O3,260β℃,反应时间4 h,400 r/min,40 mL原料 | $~{{S}_{{{\text{H}}_{\text{2}}}}}=0.65%{{S}_{\text{C}{{\text{O}}_{\text{2}}}}}=0.20\%$ $~{{S}_{\text{C}{{\text{H}}_{\text{4}}}}}=6.80%{{S}_{{{\text{C}}_{\text{2}}}{{\text{H}}_{\text{6}}}}}=0.80\%$ | 一定量甲酸、乙酸85.55%、丙酸3.78%,0.8% 乙醇,2-丁酮0.71%、2-戊酮0.97%、环戊酮3.55%、2-甲基环戊酮1.49%、3-甲基环戊酮0.42%、2-环戊酮0.56%、2-乙基环戊酮0.49%、乙酸乙酯1.2% | [20] |
| 桦木水解物 | 0.5 g Pt-Pd/C(热解沉积碳合成载体),175β℃ | $~{{S}_{{{\text{H}}_{\text{2}}}}}=0.28%{{S}_{\text{C}{{\text{O}}_{\text{2}}}}}=65\%$ $~{{S}_{\text{CO}}}<10%{{S}_{{{\text{C}}_{x}}{{\text{H}}_{y}}}}=28\%$ | — | [42] |
| 松木水解物 | 0.5 g Pt-Pd/C(热解沉积碳合成载体),175 ~ 225β℃ | $~{{S}_{{{\text{H}}_{\text{2}}}}}=22%\tilde{\ }32%{{S}_{\text{C}{{\text{O}}_{\text{2}}}}}=74%\tilde{\ }85\%$ $~{{S}_{\text{CO}}}<10%{{S}_{{{\text{C}}_{x}}{{\text{H}}_{y}}}}=10%\tilde{\ }20\%$ | — |
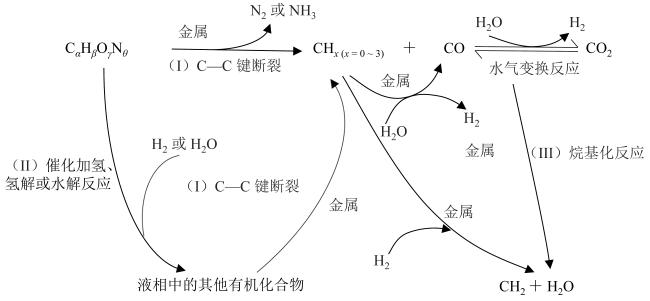
Fig. 4 Diagram of the reaction mechanism of catalytic aqueous phase reforming degradation of nitrogenous organic wastewater and hydrogen production recycling[50]: (I) C—C bond breaking; (II) catalytic hydrogenation, hydrogenolysis or hydrolysis; (III) alkylation reaction图4 催化水相重整降解含氮有机废水与制氢资源化反应机理网络图[50]:(I)C—C键断裂反应;(II)催化加氢、氢解或水解反应;(III)烷基化反应 |
3.2 藻类加工废液
3.3 生物油加工废液
3.4 废木处理废液
4 食品加工废液水相重整
4.1 淀粉加工废液
Table 6 Aqueous phase reforming reaction for waste liquid in the food industry表6 食品业废液水相重整反应 |
| 反应底物 | 反应条件 | RTOC(RCOD)/% | Si/% | 液相产物 | 参考文献 |
|---|---|---|---|---|---|
| 商用淀粉废水 | 0.4 g PtRh/C,220β℃,2.6 ~ 2.9 MPa,反应时间4 h,500 r/min,20 mL原料,pH = 5.6 ~ 9.1 | Rtoc = 99 Rcod = 99 | $~{{S}_{{{\text{H}}_{\text{2}}}}}=46.7{{S}_{\text{C}{{\text{O}}_{\text{2}}}}}=36.5$ $~{{S}_{\text{C}{{\text{H}}_{\text{4}}}}}=12.6{{S}_{{{\text{C}}_{\text{2}}}{{\text{H}}_{\text{6}}}}}=3.4$ $~{{S}_{{{\text{C}}_{\text{3}}}{{\text{H}}_{\text{8}}}}}=0.8$ | 甲酸、乙酸、丙二酸、马来酸 | [17] |
| 大米加工废水 | 0.4 g Pt/C ,220β℃,2.6 ~ 2.9 MPa,反应时间4 h,500 r/min,20 mL原料 | Rtoc = 70.9 ~ 85.4 Rcod = 99 | ${{S}_{{{\text{H}}_{\text{2}}}}}=45.4\pm 0.1$$~{{S}_{\text{C}{{\text{O}}_{\text{2}}}}}=40.4\pm 0.1$ $~{{S}_{\text{C}{{\text{H}}_{\text{4}}}}}=6.3\pm 0.1$ $~{{S}_{{{\text{C}}_{\text{2}}}{{\text{H}}_{\text{6}}}}}=4.8\pm 0.1$ $~{{S}_{{{\text{C}}_{\text{3}}}{{\text{H}}_{\text{8}}}}}=3.1\pm 0.1$ | 甲酸、马来酸 | |
| 马铃薯加工废水 | 0.4 g Pt/C,220β℃,2.6 ~ 2.9 MPa,反应时间4 h,500 r/min,20 mL原料 | Rtoc = 45.3 ~ 61.8 Rcod = 99 | ${{S}_{{{\text{H}}_{\text{2}}}}}=35.4\pm 0.1$$~{{S}_{\text{C}{{\text{O}}_{\text{2}}}}}=52.3\pm 0.1$ $~{{S}_{\text{C}{{\text{H}}_{\text{4}}}}}=10.0\pm 0.1$ $~{{S}_{{{\text{C}}_{\text{2}}}{{\text{H}}_{\text{6}}}}}=1.7\pm 0.1$ $~{{S}_{{{\text{C}}_{\text{3}}}{{\text{H}}_{\text{8}}}}}=0.6\pm 0.1$ | 甲酸、马来酸、乙酸达 400 mg/L,丙二酸249 mg/L | |
| 啤酒废水 | 0.3 g Pt/ENS350,225β℃,2.4 ~ 2.9 MPa,反应时间4 h,500 r/min,15 mL原料,pH = 9.9 | Rtoc = 80 Rcod = 85 | ${{S}_{{{\text{H}}_{\text{2}}}}}=48.9\pm 0.9$$~{{S}_{\text{C}{{\text{O}}_{\text{2}}}}}=41.7\pm 1.5$ $~{{S}_{\text{C}{{\text{H}}_{\text{4}}}}}=20.6\pm 0.6$ $~{{S}_{{{\text{C}}_{\text{2}}}{{\text{H}}_{\text{6}}}}}=3.3\pm 0.1$ | 乙醇酸酯、醋酸盐、甲酸 | [55] |
| 合成啤酒废水+碱 | 0.3 g 3% Pt/C,220β℃,2.4 ~ 2.8 MPa,反应时间4 h,500 r/min,15 mL原料,pH = 7 ~ 11 | Rtoc > 60 Rcod > 60 | ${{S}_{{{\text{H}}_{\text{2}}}}}=1.6\tilde{\ }52.7$$~{{S}_{\text{C}{{\text{O}}_{\text{2}}}}}=25.1\tilde{\ }89.6$ $~{{S}_{\text{C}{{\text{H}}_{\text{4}}}}}=6.0\tilde{\ }26.3$ | 醋酸61 ~ 117 mg/L,甲酸1 ~ 19 mg/L,羟乙酸盐或酯34 ~ 200 mg/L,氢氧化钾量视情况而定 | [43] |
| 果汁废水 | 0.3 g 3% Pt/C,220β℃,2.4 ~ 2.8 MPa,反应时间4 h,500 r/min,15 mL原料,pH = 10 | Rtoc = 60 Rcod = 50 | $~{{S}_{{{\text{H}}_{\text{2}}}}}=40.8{{S}_{\text{C}{{\text{O}}_{\text{2}}}}}=45.1$ $~{{S}_{\text{C}{{\text{H}}_{\text{4}}}}}=11.3{{S}_{{{\text{C}}_{\text{2}}}{{\text{H}}_{\text{6}}}}}=2.0$ $~{{S}_{{{\text{C}}_{\text{3}}}{{\text{H}}_{\text{8}}}}}=0.8$ | 液相产物在液体中仅剩余碳含量不到30%,主要是乙酸、甲酸和草酸 | [44] |
| 奶酪乳清 | 130 g镍基催化剂,220β℃,2.4 MPa,反应时间1 h | — | ${{S}_{{{\text{H}}_{\text{2}}}}}=11\tilde{\ }33$$~{{S}_{\text{C}{{\text{O}}_{\text{2}}}}}=49\tilde{\ }72$ ${{S}_{\text{CO}}}<2$ $~{{S}_{\text{C}{{\text{H}}_{\text{4}}}}}=7\tilde{\ }17$ | 乙醛和丙醛0 ~ 12%、2-丙酮4% ~ 100%,2-丁酮-3-羟基0 ~ 18%、乙酸和丙酸0 ~ 22%、左旋葡聚糖和D-阿洛酮、呋喃类(糠醛、2-呋喃甲醛和2,5-呋喃二甲醛)0 ~ 85%、乙醇、丙醇0 ~ 23%、1,2-丙二醇和乙二醇0 ~ 48%、酚和甲基酚 | [18] |
| 奶酪乳糖 | 10 ~ 40 g Ni-La/Al2O3,200 ~ 240β℃,3.8 ~ 5 MPa | — | ${{S}_{{{\text{H}}_{\text{2}}}}}=8\tilde{\ }60$$~{{S}_{\text{C}{{\text{O}}_{\text{2}}}}}=32\tilde{\ }88$ ${{S}_{\text{CO}}}=0\tilde{\ }15$ $~{{S}_{\text{C}{{\text{H}}_{\text{4}}}}}=0\tilde{\ }13$ | 醛类0 ~ 11%,羧酸0 ~ 22%,一元醇0 ~ 23%,多元醇0 ~ 48%,C3酮4% ~ 100%,C4酮0 ~ 18%,环酮0 ~ 15%,呋喃0 ~ 85% | [39] |
| 1%麦芽糖醇 | 0.5 g PtPd/C,175β℃,3 MPa,质量空速 = 0.12 h-1或0.3 h-1 | — | $~{{S}_{{{\text{H}}_{\text{2}}}}}\approx 80$ $~{{S}_{\text{C}{{\text{O}}_{\text{2}}}}}\approx 80$ ${{S}_{{{\text{C}}_{x}}{{\text{H}}_{y}}}}<20$ | 糖/糖醇类:葡萄糖、木糖、果糖、甘露醇、山梨糖醇、甘油醛、赤藓糖醇、丙酮、乙醇醛;酸类:乙醇酸、乳酸、甲酸、乙酸、丁酸;醇类:乙二醇、乙酰丙酸、丙二醇、异丙醇、甲醇、1-2丁二醇、乙醇;其他:羟基丙酮、甲醛、乙醛 | [30] |
| 金枪鱼烹饪废水 | 0.4 g Pt/CAPSUPER,200β℃,2.4 MPa,反应时间4 h,20 mL原料 | Rtoc = 45 ~ 60 Rcod = 45 ~ 60 | $~{{S}_{\text{C}{{\text{O}}_{\text{2}}}}}=96\tilde{\ }97$ $\begin{align} & ~{{S}_{\text{C}{{\text{H}}_{\text{4}}}}}=1.30 \\ & {{S}_{{{\text{C}}_{\text{2}}}{{\text{H}}_{\text{6}}}}}=3.50 \\ \end{align}$ | 甲酸、乙酸、磷酸、硫酸盐 | [19] |