0 引言
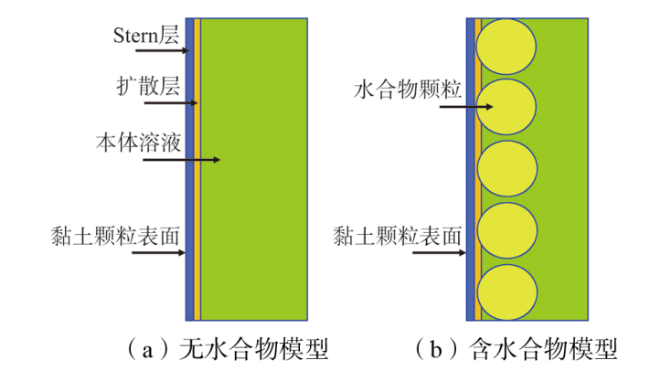
1 双电层基本理论
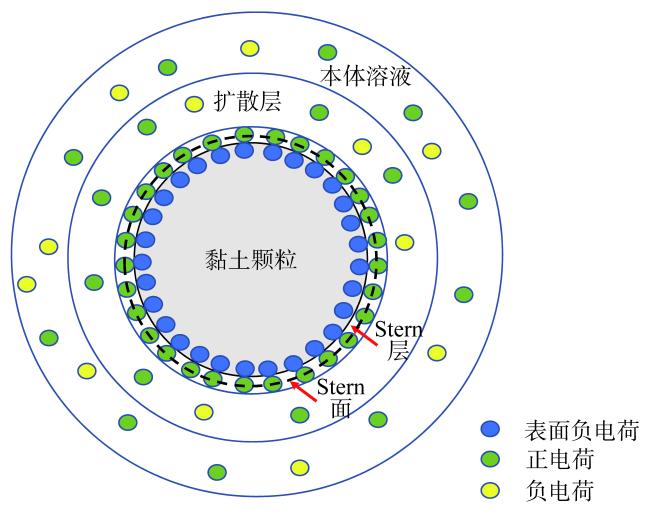
Fig. 1 Structure of electrical double layer图1 双电层结构 |
2 数值建模
2.1 分子动力学模型
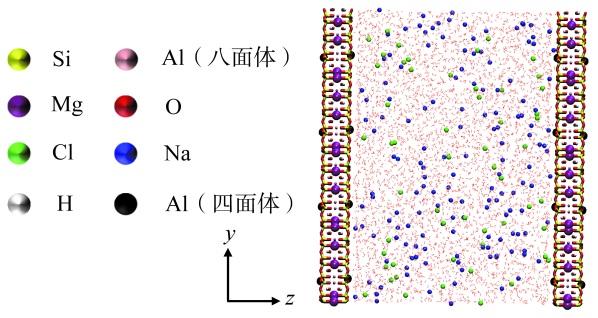
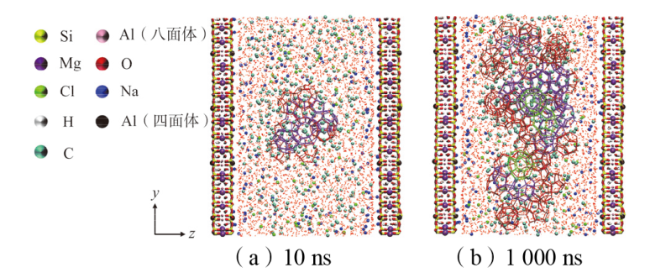
Fig. 2 Initial configuration of montmorillonite-NaCl solution mixture图2 蒙脱石-NaCl溶液混合物初始构型 |
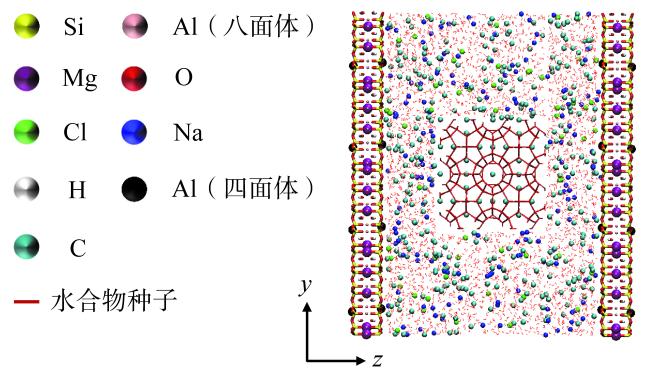
Fig. 3 Initial configuration of montmorillonite-NaCl solution-methane hydrate mixture图3 蒙脱石-NaCl溶液-甲烷水合物混合物的初始构型 |
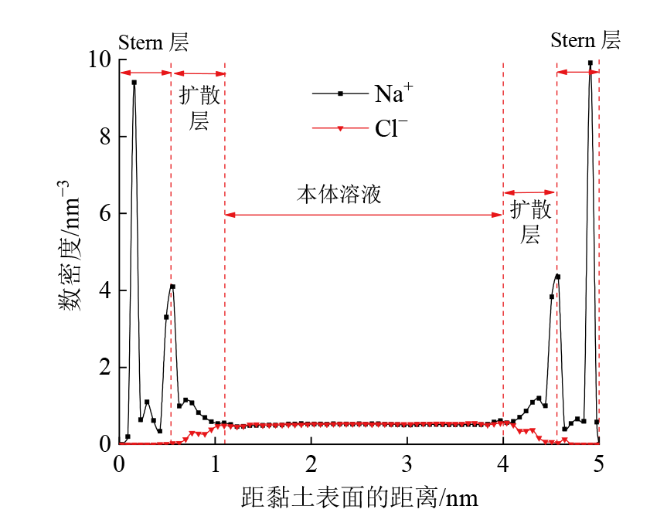
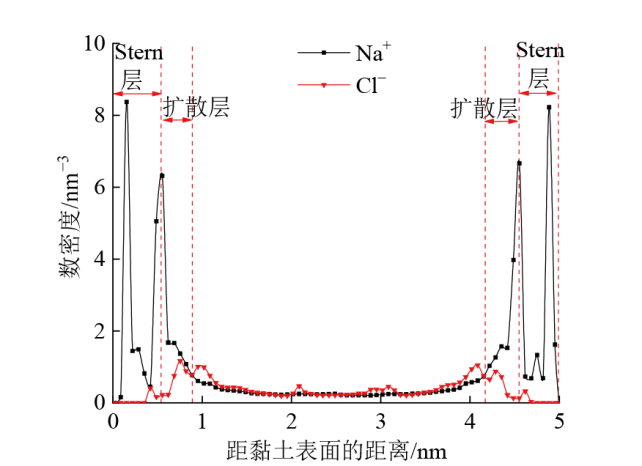
Fig. 4 Number density distribution of ions along the z direction in the hydrate-free model图4 无水合物模型中离子数密度沿z轴方向的分布 |
Table 1 Thickness of electrical double layer in hydrate-free model表1 无水合物模型的双电层厚度 |
| 电层 | 理论估计值/nm | 左侧黏土层/nm | 右侧黏土层/nm |
|---|---|---|---|
| Stern层 | 0.36 | 0.54 | 0.44 |
| 扩散层 | 0.70 | 0.56 | 0.56 |
2.2 有限元数值模型
Fig. 5 Two-dimensional geometric structure of electrical double layer on the surface of montmorillonite图5 蒙脱石表面双电层的二维几何结构 |
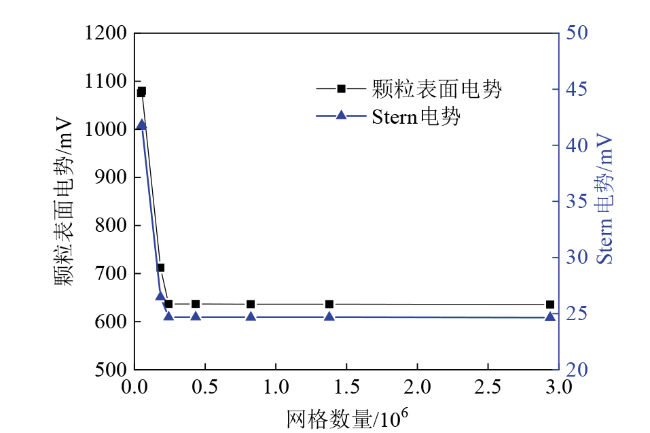
Fig. 6 Variation curves of the surface potential of clay particle and Stern potential with the number of grids图6 黏土颗粒表面电势与Stern电势随网格数量变化曲线 |
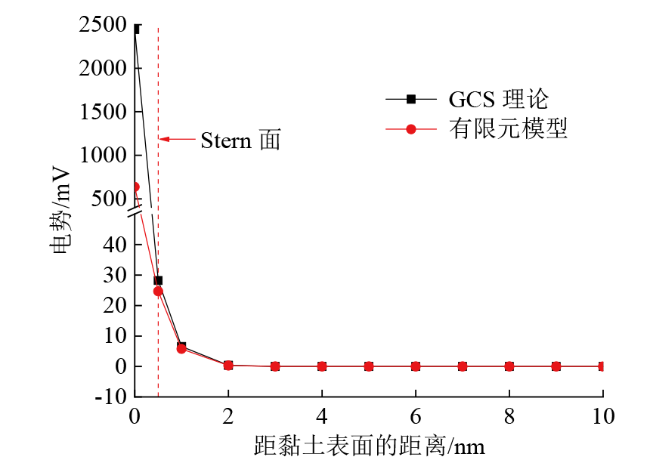
Fig. 7 Comparison of potential distribution between GCS theory and finite element model图7 GCS理论与有限元模型的电势分布对比 |
3 结果分析
3.1 数值模拟中水合物的形成
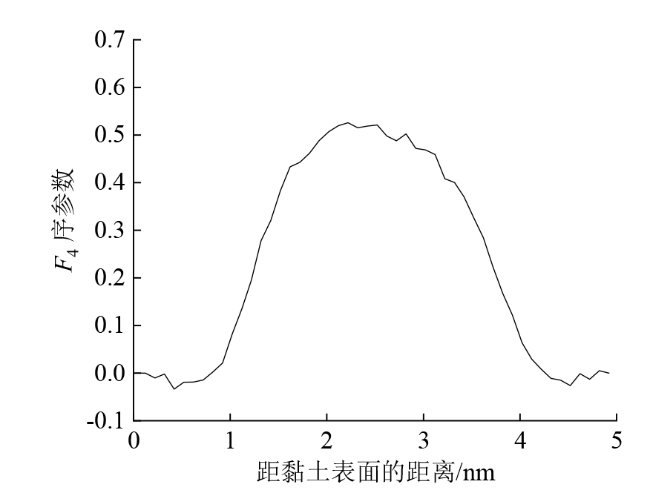
Fig. 8 Variation trend of F4 order parameter along the z direction图8 F4序参数沿z轴方向的变化趋势 |
Fig. 9 Growth process of hydrate图9 水合物生长过程 |
3.2 双电层结构和离子扩散系数
Fig.10 Number density distribution of ions along the z direction in the hydrate-bearing model图10 含水合物模型中离子数密度沿z轴方向的分布 |
Table 2 Thickness of electrical double layer in hydrate-bearing model表2 含水合物模型的双电层厚度 |
| 电层 | 左侧黏土层/nm | 右侧黏土层/nm |
|---|---|---|
| Stern层 | 0.54 | 0.45 |
| 扩散层 | 0.35 | 0.33 |
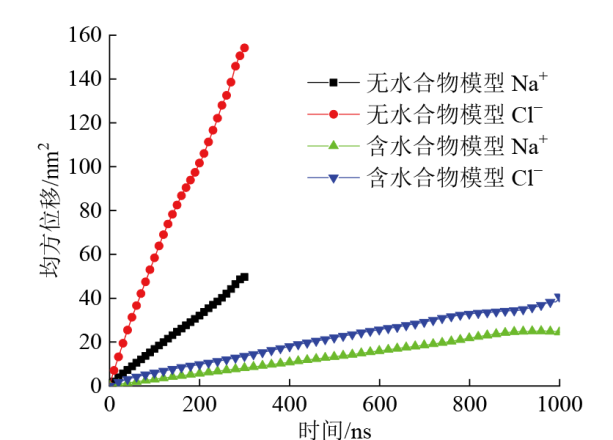
Fig. 11 Curve of ions mean squared displacement variation with time图11 离子的均方位移随时间变化曲线 |
Table 3 Diffusion coefficients of ions表3 离子的扩散系数 |
| 模型 | ${{D}_{\text{N}{{\text{a}}^{\text{+}}}}}$/(m2/s) | ${{D}_{\text{C}{{\text{l}}^{-}}}}$/(m2/s) |
|---|---|---|
| 无水合物 | 2.6 × 10-11 | 7.7 × 10-11 |
| 含水合物 | 4.3 × 10-12 | 6.5 × 10-12 |
3.3 双电层内电势分布
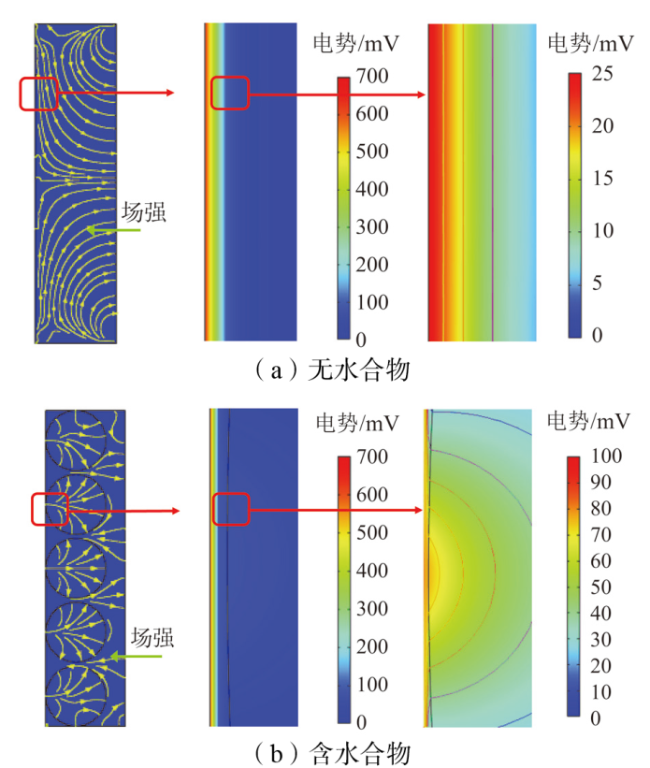
Fig. 12 Cloud images of potential distribution in hydrate-free system and hydrate-bearing system图12 无水合物体系与含水合物体系的电势分布云图 |
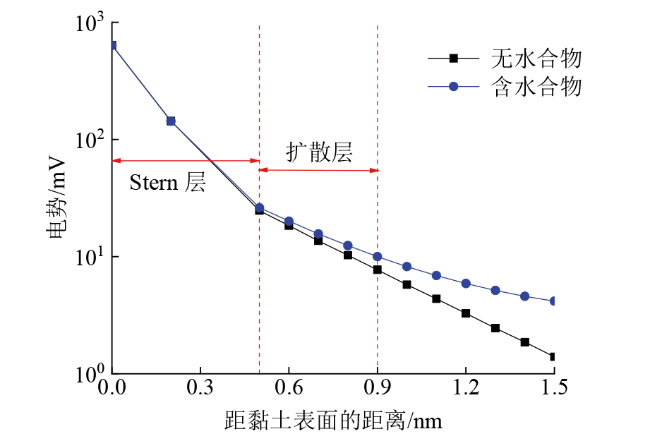
Fig. 13 Comparison of average potential distribution near the surface of clay particle in hydrate-free system and hydrate-bearing system图13 无水合物体系与含水合物体系中黏土颗粒表面附近的平均电势分布对比 |
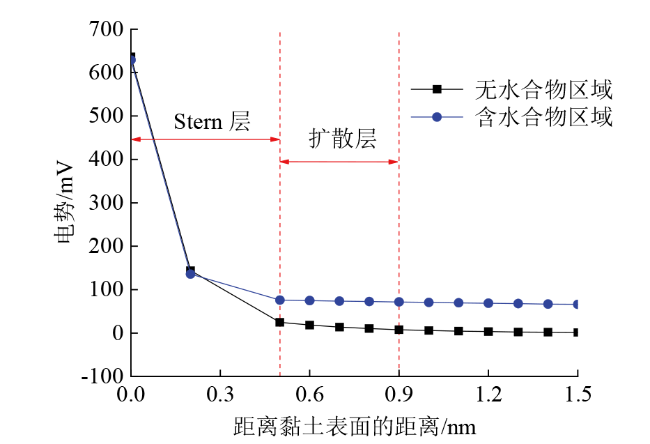
Fig. 14 Average potential distribution in the hydrate-free region and hydrate-bearing region of the hydrate-bearing system图14 含水合物体系中无水合物区域和含水合物区域的平均电势分布 |
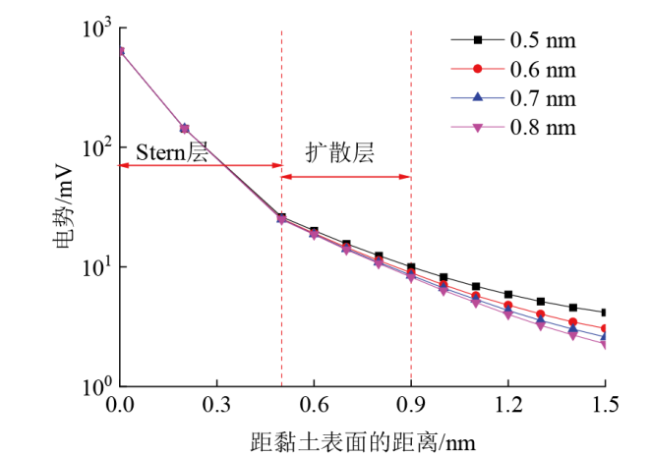
Fig. 15 Average potential distribution near the surface of clay particles with the hydrate at different positions图15 水合物在不同位置时黏土颗粒表面附近的平均电势分布 |