0 前言
1 水合物法分离CO2工艺
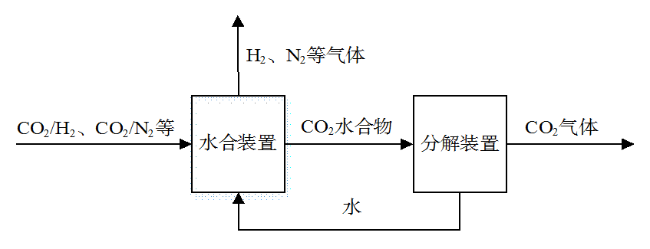
1.1 基本原理及重要参数
Fig. 1 Schematic diagram of hydrate-based CO2 separation图1 水合物法分离CO2示意图 |
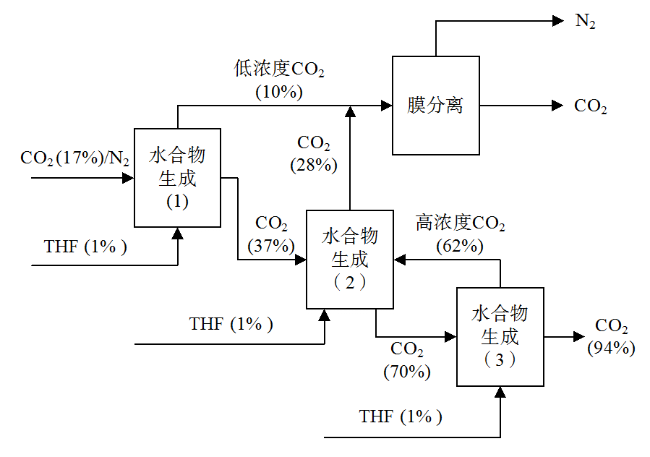
1.2 工艺研究
Table 1 Effect of different promoters on CO2 separation from CO2/N2表1 不同促进剂对分离CO2/N2中CO2的影响 |
| 气体组分 | 温度 / K | 压力 / MPa | 促进剂(摩尔浓度) | 气体消耗量 / mol | 分离因子 | 参考文献 |
|---|---|---|---|---|---|---|
| 16.9% CO2 + 83.1% N2 | 273.70 | 1.50 | THF (1.00%) | 0.360 0 | 4.12 | [17] |
| 273.70 | 2.50 | THF (1.00%) | 0.660 0 | 4.31 | ||
| 273.70 | 2.30 | THF (1.50%) | 0.590 0 | 3.88 | ||
| 16.9% CO2 + 83.1% N2 | 277.65 | 5.33 | TBAF (0.29%) | 0.060 5 | 6.75 | [18] |
| 277.65 | 5.49 | TBAF (0.29%) | 0.043 0 | 24.30 | ||
| 280.25 | 4.42 | TBAF (0.29%) | 0.070 0 | 22.15 | ||
| 17.0% CO2 + 83.0% N2 | 276.65 | 1.00 | TBAB (0.29%) | 0.010 7 | 9.72 | [19] |
| 276.65 | 2.00 | TBAB (0.29%) | 0.011 3 | 12.68 | ||
| 65.0% CO2 + 35.0% N2 | 276.50 | 1.00 | TBAB (0.29%) | 0.013 2 | 5.94 | |
| 276.50 | 2.00 | TBAB (0.29%) | 0.013 7 | 7.16 | ||
| 17.0% CO2 + 83.0% N2 | 275.14 | 2.50 | TBANO3 (1.00%) | 0.070 0 | 15.54 | [20] |
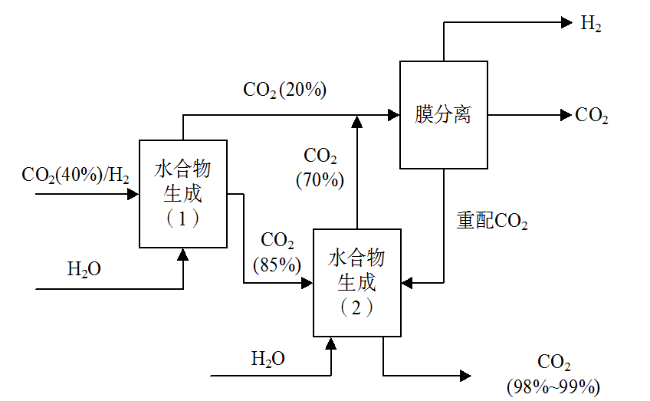
Table 2 Effect of different promoters on CO2 separation from CO2/H2表2 不同促进剂对分离CO2/H2中CO2的影响 |
| 气体组分 | 温度 / K | 压力 / MPa | 促进剂(摩尔浓度) | 气体消耗量 / mol | 分离因子 | 参考文献 |
|---|---|---|---|---|---|---|
| 40.0% CO2 + 60.0% H2 | 284.15 | 3.00 | TBAB (0.5%) | 0.017 1 | 16.11 | [21] |
| 286.15 | 3.00 | TBAB (1.0%) | 0.030 8 | 25.99 | ||
| 287.85 | 3.00 | TBAB (3.0%) | 0.013 7 | 20.23 | ||
| 40.0% CO2 + 60.0% H2 | 277.15 | 4.50 | THF (1.0%) | 0.015 0 | 14.30 | [22] |
| 277.15 | 4.50 | TH F (1.0%) + 环己烷 (10.0%体积浓度) | 0.015 1 | 41.40 | ||
| 39.9% CO2 + 60.1% H2 | 279.60 | 4.59 | THF (0.5%) | 0.003 6 | - | [23] |
| 279.60 | 3.14 | THF (1.0%) | 0.017 4 | - | ||
| 279.60 | 1.55 | THF (3.0%) | 0.011 2 | - |
1.3 水合物生成分离装置
Table 3 Effect of different hydrate formation devices on CO2 separation表3 不同的水合物生成装置对分离CO2的影响 |
| 反应器类型 | 温度 / K | 压力 / MPa | 促进剂(质量浓度) | 其他参数 | 气体消耗量 / mol | 分离因子 | 参考文献 |
|---|---|---|---|---|---|---|---|
| 搅拌反应器 | 274.55 | 5.0 | SDS (300.0 mg/kg) | 搅拌速度 (100 r/min) | - | 5.68 | [32] |
| 搅拌诱导结晶器 | 274.25 | 2.3 | THF (1.5%,摩尔浓度) | 搅拌速度 (400 r/min) | 0.016 | 3.88 | [17] |
| 固定床反应器 | 274.65 | 3.0 | SDS (1.0%) | 无填料 | 0.093 | - | [33] |
| 274.65 | 3.0 | SDS (1.0%) | 填料:SSP-1 | 0.084 ~ 0.079 | - | ||
| 274.65 | 3.0 | SDS (1.0%) | 填料:硅胶 | 0.059 ~ 0.067 | - | ||
| 274.65 | 3.0 | SDS (1.0%) | 填料:硅砂 | 0.093 ~ 0.096 | - | ||
| 固定床反应器 | 274.65 | 3.0 | SDS (0.5%) | 填料:5A沸石 | 0.024 ~ 0.027 | - | [34] |
| 274.65 | 3.0 | SDS (0.5%) | 填料:13X沸石 | 0.088 ~ 0.091 | - | ||
| 274.65 | 3.0 | SDS (0.5%) | 填料:硅砂 | 0.090 ~ 0.114 | - | ||
| 固定床反应器 | 272.15 | 5.0 | THF (1.5%,摩尔浓度) | 填料:硅胶 | 0.018 | 7.82 | [35] |
| 固定床反应器 | 274.20 | 6.0 | THF (1.0%,摩尔浓度) | 填料:煤颗粒 | 0.179 | 10.00 | [36] |
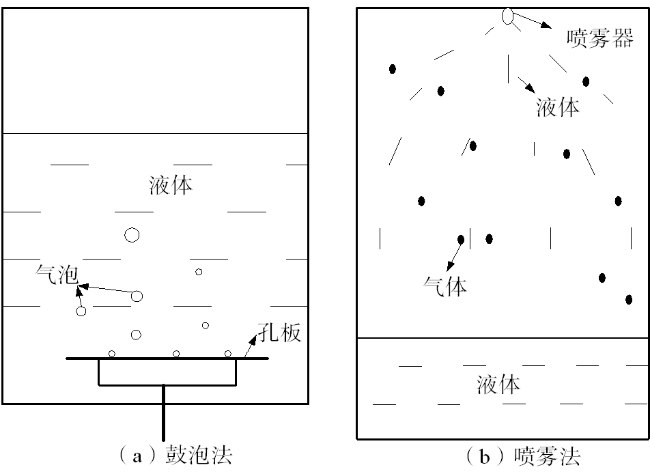
Fig. 4 Bubble method and spray method图4 鼓泡法和喷雾法 |