0 引言
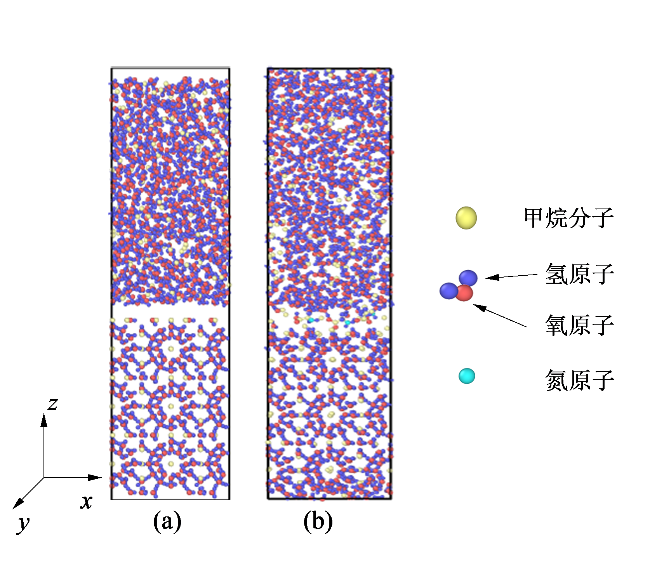
1 模型与方法
表1 PVCap、甘氨酸及其短肽的分子结构Table 1 The molecular structures of PVCap, glycine, and its short peptides |
| 动力学 抑制剂 | 分子式 | 分子结构 | 相对分子质量 |
|---|---|---|---|
| PVCap | C24H41O3N3 | 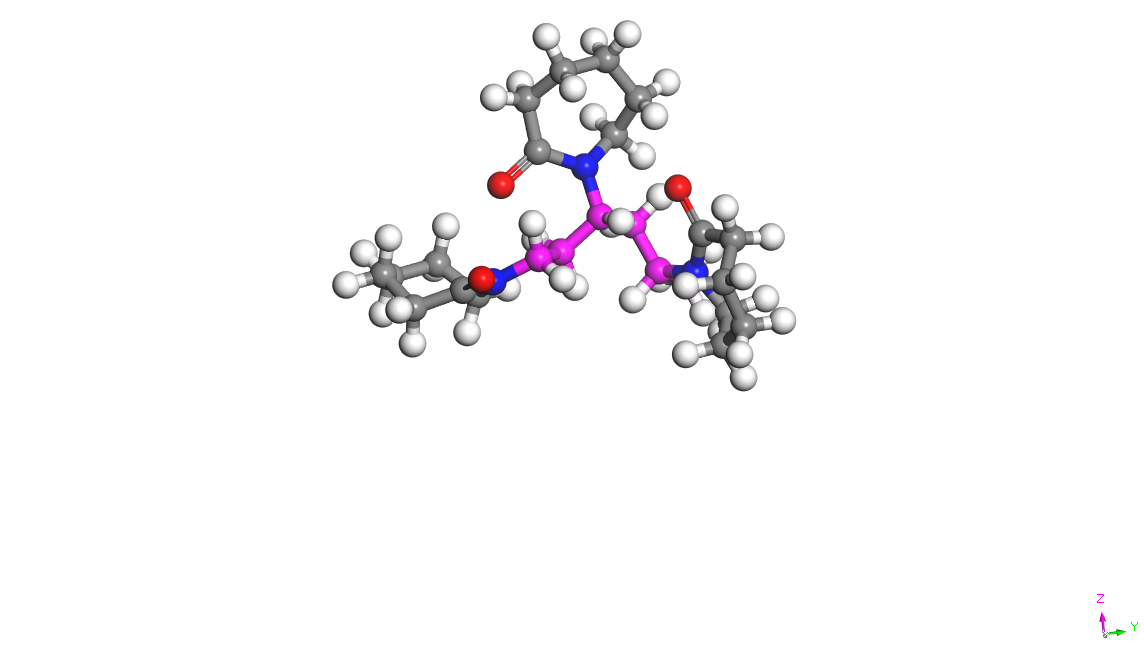 | 419 |
| gly | C2H5O2N | 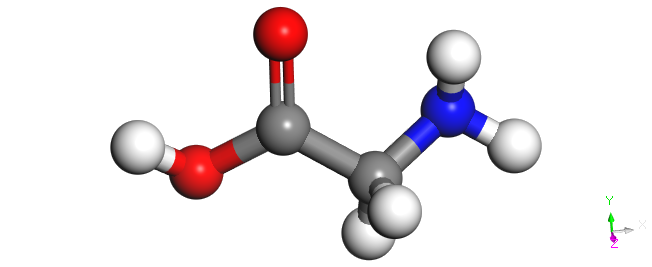 | 75 |
| 3G | C6H11O4N3 | 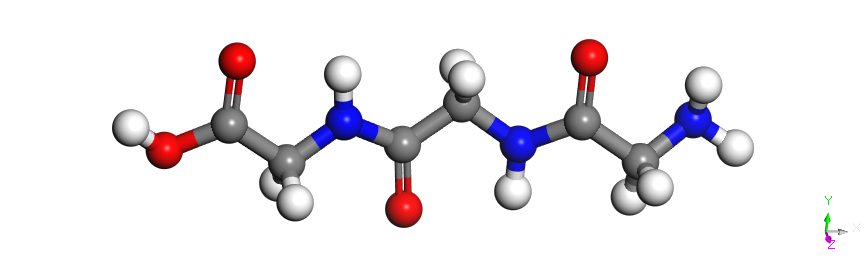 | 189 |
| 5G | C10H17O6N5 | 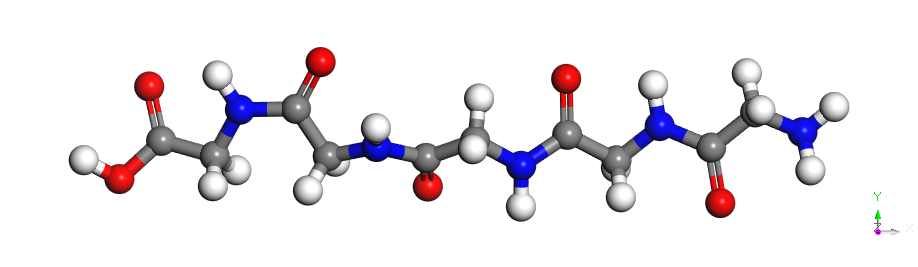 | 303 |
2 结果与讨论
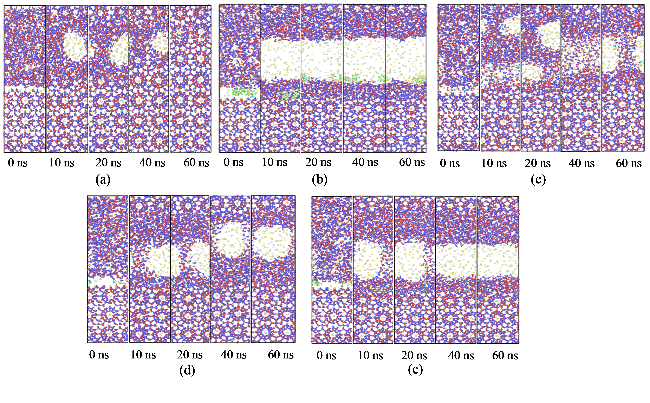
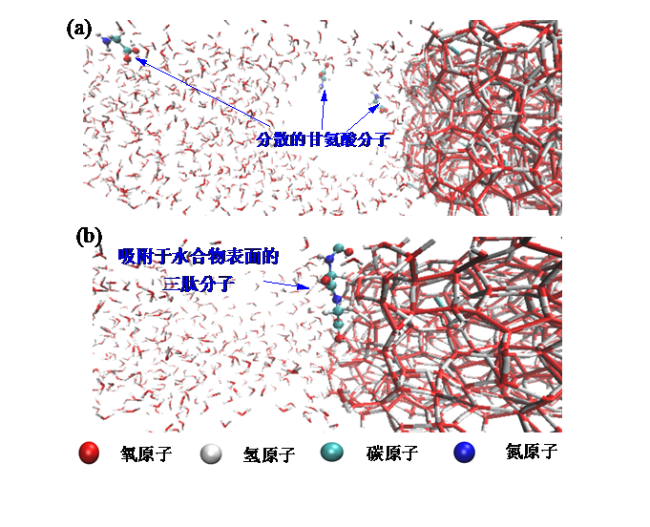
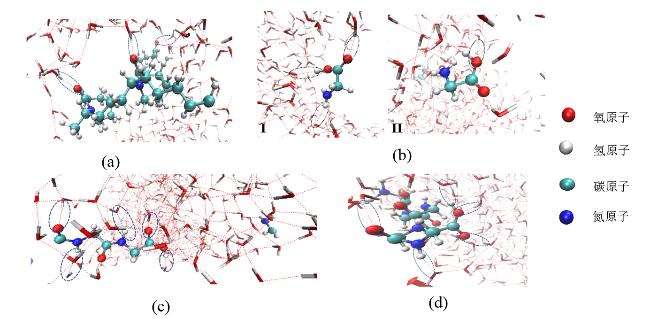
2.1 水合物生长构象
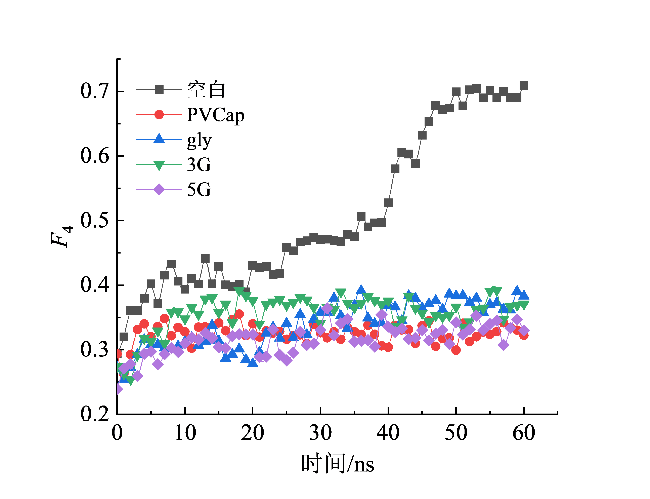
2.2 水合物生长结构参数
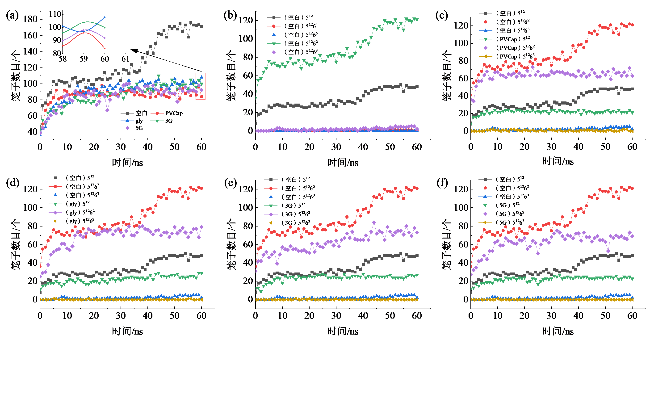
图5 水合物笼子数目随时间变化:(a)不同体系水合物笼子总数;(b)空白体系不同类型笼子;(c)空白与PVCap体系;(d)空白与gly体系;(e)空白与3G体系;(f)空白与5G体系Fig. 5 Number of hydrate cages over time: (a) total number of hydrate cages in different systems; (b) different types of cages in blank system; (c) blank and PVCap systems; (d) blank and gly systems; (e) blank and 3G systems; (f) blank and 5G systems |