0 引言
1 实验部分
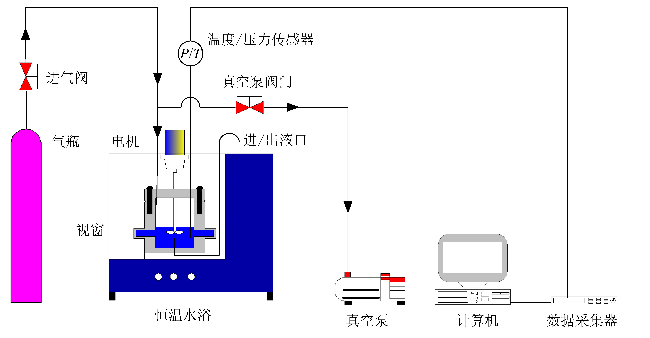
1.1 实验仪器和材料
1.2 实验步骤
1.3 数据分析方法
2 结果和讨论
2.1 [BMIM][OS]离子液体的CO2溶解度
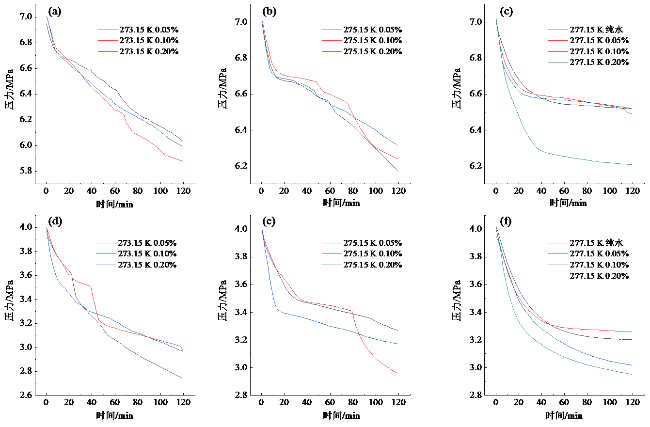
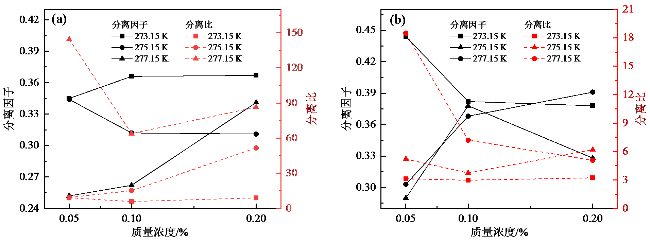
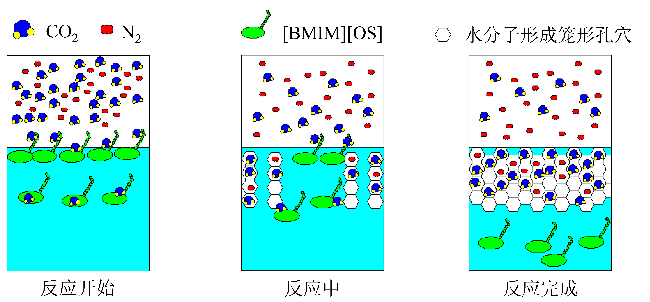
2.2 [BMIM][OS]离子液体对水合物形成动力学的影响
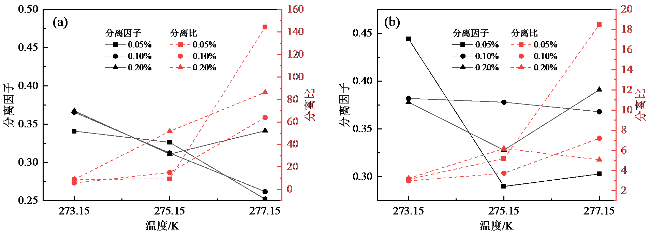
表1 不同运行条件下[BMIM][OS]作为添加剂处理二元混合气体水合物的气体分离实验结果Table 1 Gas separation experimental results using [BMIM][OS] as additives for binary mixture gas hydrate under different operating conditions |
| 实验条件 | 序号 | 温度/K | 离子液体质量浓度/% | 过冷度/K | 气体摩尔比例 | ${{S}_{C{{O}_{2}}}}$ | F |
|---|---|---|---|---|---|---|---|
| 体系1 P = 7.0 MPa | 1 | 273.15 | 0.05 | 7.60 | 44.8/55.2 | 0.34 | 9.03 |
| 2 | 275.15 | 0.05 | 5.60 | 43.8/56.2 | 0.33 | 9.44 | |
| 3 | 277.15 | 0.05 | 3.60 | 45.6/54.4 | 0.25 | 144.40 | |
| 4 | 273.15 | 0.10 | 7.60 | 44.8/55.2 | 0.37 | 5.84 | |
| 5 | 275.15 | 0.10 | 5.60 | 45.2/54.8 | 0.31 | 15.09 | |
| 6 | 277.15 | 0.10 | 3.60 | 45.7/54.3 | 0.26 | 63.89 | |
| 7 | 273.15 | 0.20 | 7.60 | 44.0/56.0 | 0.37 | 9.01 | |
| 8 | 275.15 | 0.20 | 5.60 | 44.7/55.3 | 0.31 | 51.70 | |
| 9 | 277.15 | 0.20 | 3.60 | 43.6/56.4 | 0.34 | 86.42 | |
| 10 | 277.15 | 0.00 | 3.60 | 45.7/54.3 | 0.18 | 8.05 | |
| 体系2 P = 4.0 MPa | 11 | 273.15 | 0.05 | 7.60 | 73.6/26.4 | 0.44 | 3.13 |
| 12 | 275.15 | 0.05 | 5.60 | 75.4/24.6 | 0.29 | 5.20 | |
| 13 | 277.15 | 0.05 | 3.60 | 74.0/26.0 | 0.30 | 18.49 | |
| 14 | 273.15 | 0.10 | 7.60 | 74.9/25.1 | 0.38 | 2.98 | |
| 15 | 275.15 | 0.10 | 5.60 | 74.3/25.7 | 0.38 | 3.74 | |
| 16 | 277.15 | 0.10 | 3.60 | 73.2/26.8 | 0.37 | 7.20 | |
| 17 | 273.15 | 0.20 | 7.60 | 74.7/25.3 | 0.38 | 3.23 | |
| 18 | 275.15 | 0.20 | 5.60 | 74.4/25.6 | 0.33 | 6.18 | |
| 19 | 277.15 | 0.20 | 3.60 | 72.1/27.9 | 0.40 | 8.49 | |
| 20 | 277.15 | 0.00 | 3.60 | 73.0/27.0 | 0.33 | 51.98 |
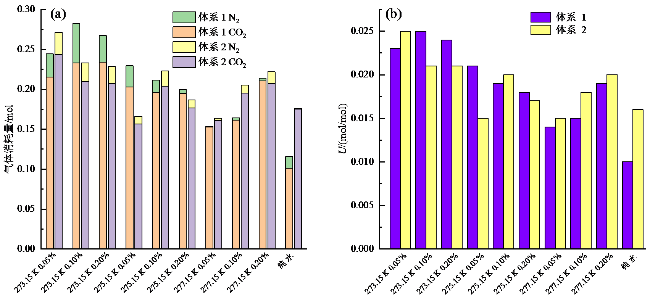
表2 不同运行条件下的CO2、N2和气体消耗总量Table 2 CO2, N2 and total gas consumptions under different operating conditions |
| 实验条件 | 序号 | CO2消耗量/mol | ${{U}_{C{{O}_{2}}}}$/(mol/mol) | N2消耗量/mol | ${{U}_{{{N}_{2}}}}$/(mol/mol) | 气体消耗总量/mol | $U$/(mol/mol) |
|---|---|---|---|---|---|---|---|
| 体系1 P = 7.0 MPa | 1 | 0.220 | 0.020 | 0.033 | 0.003 | 0.253 | 0.023 |
| 2 | 0.203 | 0.019 | 0.026 | 0.001 | 0.229 | 0.021 | |
| 3 | 0.153 | 0.014 | 0.001 | 0.000 | 0.154 | 0.014 | |
| 4 | 0.233 | 0.021 | 0.049 | 0.004 | 0.282 | 0.025 | |
| 5 | 0.196 | 0.018 | 0.016 | 0.001 | 0.211 | 0.019 | |
| 6 | 0.161 | 0.015 | 0.003 | 0.000 | 0.164 | 0.015 | |
| 7 | 0.234 | 0.021 | 0.033 | 0.003 | 0.267 | 0.024 | |
| 8 | 0.195 | 0.018 | 0.005 | 0.000 | 0.200 | 0.018 | |
| 9 | 0.210 | 0.019 | 0.003 | 0.000 | 0.214 | 0.019 | |
| 10 | 0.101 | 0.009 | 0.015 | 0.001 | 0.116 | 0.010 | |
| 体系2 P = 4.0 MPa | 11 | 0.243 | 0.022 | 0.028 | 0.003 | 0.271 | 0.025 |
| 12 | 0.156 | 0.014 | 0.010 | 0.001 | 0.166 | 0.015 | |
| 13 | 0.161 | 0.014 | 0.003 | 0.000 | 0.164 | 0.015 | |
| 14 | 0.209 | 0.019 | 0.024 | 0.002 | 0.233 | 0.021 | |
| 15 | 0.204 | 0.018 | 0.019 | 0.002 | 0.223 | 0.020 | |
| 16 | 0.195 | 0.018 | 0.010 | 0.001 | 0.205 | 0.018 | |
| 17 | 0.207 | 0.019 | 0.022 | 0.002 | 0.229 | 0.021 | |
| 18 | 0.177 | 0.016 | 0.010 | 0.001 | 0.187 | 0.017 | |
| 19 | 0.212 | 0.019 | 0.010 | 0.001 | 0.222 | 0.020 | |
| 20 | 0.175 | 0.016 | 0.001 | 0.000 | 0.176 | 0.016 |