0 前言
1 实验与方法
1.1 实验原料
Table 1 Properties of activated sludge表 1 活性污泥基本性质 |
| Sample | pH | Moisture / % | VSS/TSS | CST / s | Zeta potential / mV | SCOD / (mg/L) | SV30 / % |
|---|---|---|---|---|---|---|---|
| WAS | 6.87 | 99.43 | 0.66 | 11.90 | -14.20 | 32.00 | 18.50 |
Table 2 Proximate analysis and elemental analysis of sludge cake表 2 污泥泥饼工业分析与元素分析 |
| Sample | Proximate analysis / % | Elemental analysis / % | |||||||
|---|---|---|---|---|---|---|---|---|---|
| Moisture | Asha | Volatile mattera | Fixed carbon | C | H | N | S | ||
| SS | 78.61 | 63.24 | 33.50 | 3.26 | 16.01 | 3.02 | 2.53 | 0.88 | |
Note: a dry basis. |
1.2 实验试剂及仪器
1.3 污泥基生物炭的制备
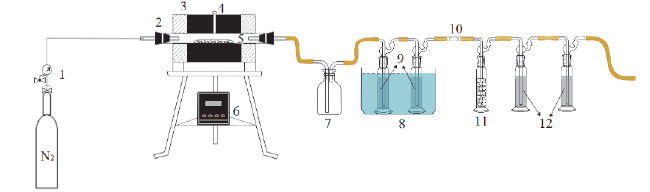
Fig. 1 A schematic of the experimental system: 1-flowmeter; 2-rubber plug; 3-horizontal tubular quartz reactor; 4-thermocouple, 5-railboat; 6-temperature controller; 7-gas bottle; 8-shaker incubator; 9,12-tail gas absorber; 10-cotton filter; 11-anhydrous calcium chloride图1 热解装置示意图:1-流量计;2-橡胶塞;3-水平石英管加热装置;4-热电偶;5-石英舟;6-温控装置;7-集气瓶;8-水浴槽;9、12-尾气吸收瓶;10-石英棉过滤器;11-无水氯化钙 |
Table 3 Ratio of activator to sludge表3 活化剂与污泥配比情况 |
| Modifiers | mSS:mmodifier | Washing method | Marked |
|---|---|---|---|
| FeCl3 | 3:4 | water | FeCl3 |
| ZnCl2 | 3:2 | water | ZnCl2 |
| CH3COOK | 1:2 | water | CH3COOK |
| H2SO4 | 5:9 | NaOH +water | H2SO4 5:9 |
| H2SO4 | 1:2 | NaOH + water | H2SO4 1:2 |
| H3PO4 | 1:3 | NaOH + water | H3PO4 |
| KOH | 1:2 | HCl + water | KOH |
| CO2 | / | / | CO2 |
| N2 | / | / | N2 |
1.4 污泥基生物炭调理性能实验
1.5 分析方法
2 结果与讨论
2.1 生物炭物理特性
Table 4 Specific surface area of different activated sludge biochar表 4 污泥基生物炭氮吸附比表面积孔径分析 |
| Modifiers | BET surface area / (m2/g) | Vtotal / (cm3/g) | Average pore width / nm |
|---|---|---|---|
| FeCl3 | 127.147 | 0.181 | 77.002 |
| ZnCl2 | 180.273 | 0.283 | 71.003 |
| CH3COOK | 50.205 | 0.101 | 79.238 |
| H2SO4 1:2 | 1 332.732 | 4.325 | 78.124 |
| H2SO4 5:9 | 154.637 | 0.526 | 68.093 |
| H3PO4 | 117.087 | 0.266 | 103.209 |
| KOH | 79.808 | 0.239 | 32.334 |
| CO2 | 65.388 | 0.194 | 65.145 |
| N2 | 25.924 | 0.117 | 127.836 |
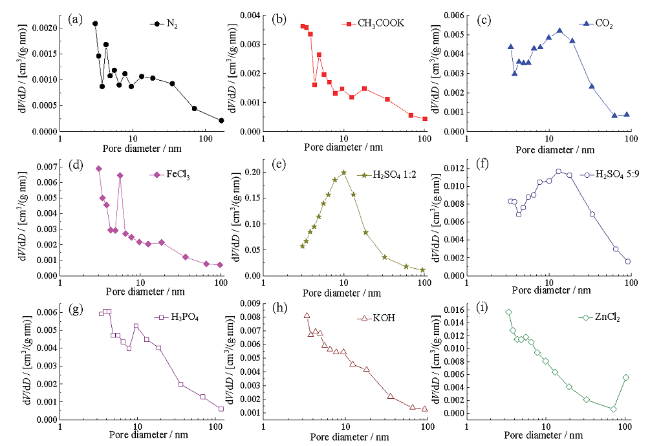
Fig. 2 BJH pore size distribution of different modified biochar图2 不同活化生物炭孔径分布 |
Table 5 The main elements of sludge-based biochars表5 污泥基生物炭主要元素 |
| Modifiers | Element content / % | |||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| Al | Fe | P | Ca | K | S | Na | Mg | Zn | Co | |
| FeCl3 | 11.506 | 8.875 | 4.954 | 1.151 | 1.438 | 1.209 | / | / | / | / |
| ZnCl2 | 10.707 | 6.569 | 3.826 | 1.929 | 0.925 | 1.377 | 1.277 | / | 7.480 | / |
| CH3COOK | 8.518 | 6.070 | 2.601 | 1.953 | 10.442 | 0.720 | / | / | / | / |
| H2SO4 1:2 | 12.964 | 9.268 | 5.514 | 2.779 | 0.757 | 1.947 | / | / | / | 1.172 |
| H2SO4 5:9 | 11.538 | 6.980 | 4.223 | 2.270 | 0.737 | 1.269 | 0.714 | / | / | / |
| CO2 | 11.825 | 8.818 | 5.186 | 2.775 | 1.569 | 1.267 | / | 0.659 | / | / |
| N2 | 10.830 | 16.455 | 6.221 | 3.696 | 3.000 | 0.986 | / | / | / | / |
| H3PO4 | 7.911 | 7.008 | 8.654 | 1.921 | 0.418 | / | 5.760 | / | / | / |
| KOH | 9.870 | 5.933 | 2.884 | 1.221 | 13.732 | / | / | / | / | / |
Fig. 3 Scanning electron microscopy of different modified biochar: (a) FeCl3-activated; (b) ZnCl2-activated; (c) CH3COOK-activated; (d) H2SO4 1:2-activated; (e) H2SO4 5:9-activated; (f) H3PO4-activated; (g) KOH-activated; (h) CO2-activated; (i) N2-activated图3 不同活化生物炭扫描电镜图:(a)FeCl3活化;(b)ZnCl2 活化;(c)CH3COOK活化;(d)H2SO4 1:2活化;(e)H2SO4 5:9活化;(f)H3PO4 活化;(g)KOH 活化;(h)CO2 活化;(i)N2活化 |
2.2 生物炭有机特征
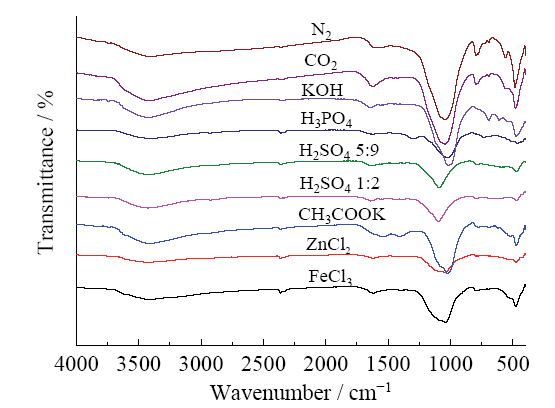
Fig. 4 Fourier-transform infrared spectra of different modified biochar图4 不同活化生物炭傅里叶红外光谱图 |
2.3 不同活化生物炭调理后的脱水性能
Table 6 Biochar conditioning modified sludge dosage表6 生物炭调理活性污泥投加量 |
| Samples | Dosage / g | WAS / mL |
|---|---|---|
| FeCl3 | 1.0 | 100 |
| ZnCl2 | 0.8 | 100 |
| CH3COOK | 0.9 | 100 |
| H2SO4 1:2 | 1.0 | 100 |
| H2SO4 5:9 | 1.1 | 100 |
| H3PO4 | 0.8 | 100 |
| KOH | 1.0 | 100 |
| CO2 | 0.9 | 100 |
| N2 | 1.0 | 100 |
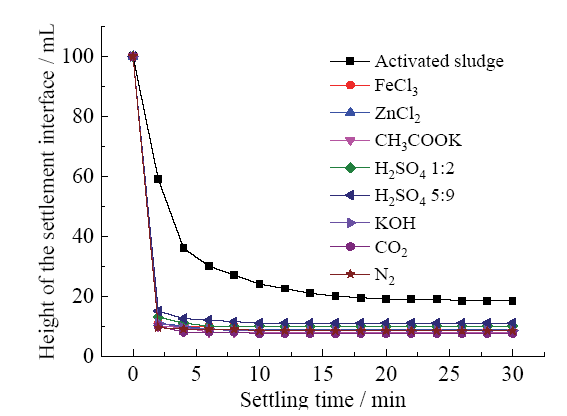
Fig. 5 Settlement curves of sewage sludge with different modified biochar图5 活化生物炭调理活性污泥时间-液面高度曲线 |
Table 7 Settling velocity of different biochar conditioning activities表7 不同污泥基生物炭调理活性污泥沉降比 |
| Samples | SV30 / % |
|---|---|
| WAS | 18.5 |
| FeCl3 | 10.0 |
| ZnCl2 | 9.0 |
| CH3COOK | 8.0 |
| H2SO4 1:2 | 10.0 |
| H2SO4 5:9 | 11.0 |
| H3PO4 | / |
| KOH | 8.5 |
| CO2 | 7.5 |
| N2 | 8.5 |
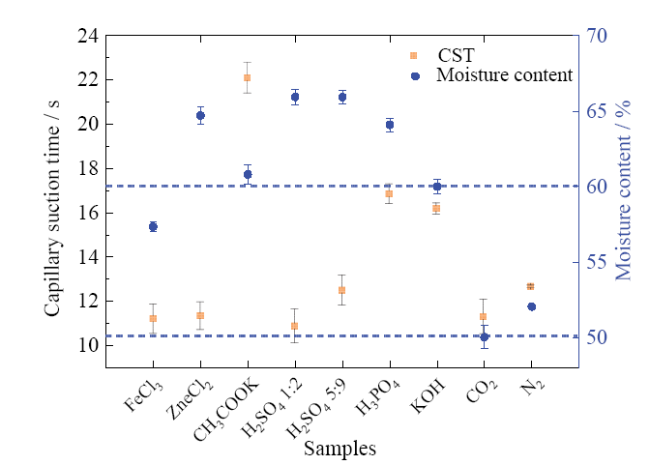
Fig. 6 CST and cake moisture content of activated sludge with different modified biochar图6 不同活化生物炭调理活性污泥CST和泥饼含水率 |