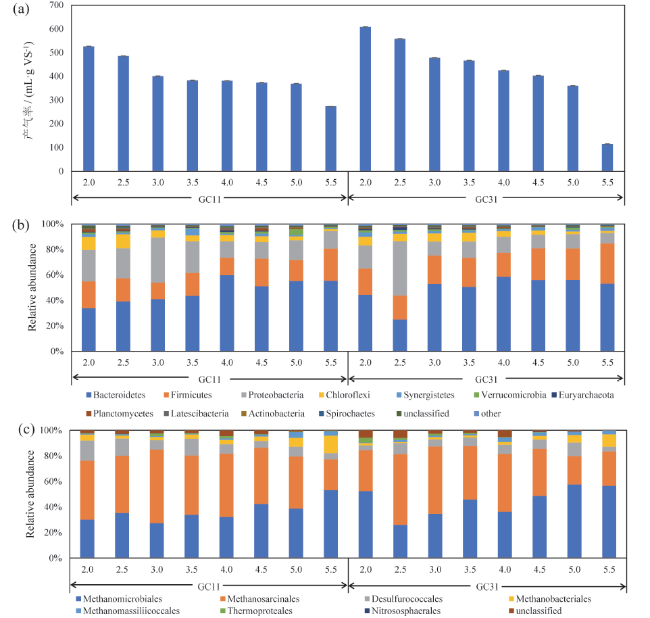
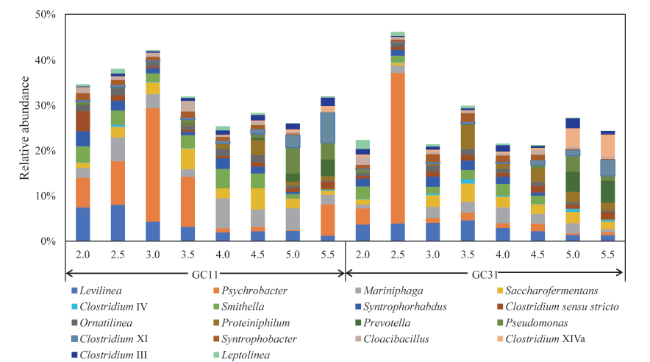
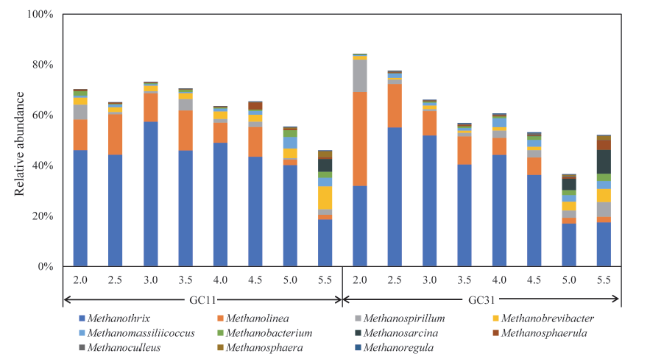
对于GC11系统,随着有机负荷从2.0 g VS/(L∙d)逐步增加至5.5 g VS/(L∙d),长蝇菌属(
Levilinea)、
Ornatilinea、排污管竿菌属(
Cloacibacillus)和纤蝇菌属(
Leptolinea)的相对丰度分别从7.37%降至1.20%、从1.35%降至0.14%、从1.17%降至0.21%和从0.45%降至0.13%;对于GC31系统,随着有机负荷升高,这4种菌属的相对丰度从3.68%降至1.30%、从0.65%降至0.29%、从1.81%降至0.58%和从1.99%降至0.04%。长蝇菌属、
Ornatilinea、排污管竿菌属、纤蝇菌属均能参与蛋白质和氨基酸物质的转化。在GC11和GC31系统中,它们的相对丰度都呈现随着系统有机负荷的升高而降低的趋势。长蝇菌属可在pH值6.0 ~ 7.2时发酵糖类和氨基酸,其主要产物是H
2、乙酸和乳酸;
Ornatilinea可代谢多肽类和碳水化合物(包括微晶态纤维素),生长适宜pH值为7.5 ~ 8.0
[22];而排污管竿菌属和纤蝇菌属都是蛋白和氨基酸降解菌
[23,24]。在GC11系统中,当系统有机负荷低于4.5 g VS/(L∙d) 时,假单胞菌属(
Pseudomonas)的相对丰度为0.06% ~ 0.93%,在5.0 ~ 5.5 g VS/(L∙d) 时相对丰度升高至3.68% ~ 5.78%;而在GC31系统中,该菌属的相对丰度则从系统有机负荷低于4.5 g VS/(L·d) 时的0.11% ~ 0.83%显著升至有机负荷为5.0 ~ 5.5 g VS/(L∙d) 时的1.07% ~ 3.54%,增幅可达29% ~ 3118%。当有机负荷从2.0 g VS/(L∙d) 升至5.5 g VS/(L∙d) 时,噬蛋白质菌属(
Proteiniphilum)的相对丰度从0.00%升高至1.01% ~ 1.67%,且分别在有机负荷4.5 g VS/(L∙d) (GC11)和3.5 g VS/(L∙d) (GC31)时获得了最高的相对丰度,分别为3.36%和5.34%。假单胞菌属和噬蛋白质菌属与系统中氨氮积累有关。假单胞菌属可代谢葡萄糖和木糖,并且可分泌胞外蛋白酶强化不溶性蛋白的水解
[25]。噬蛋白质菌属是专性厌氧蛋白质水解菌,可水解发酵酵母提取物、蛋白胨、丙酮酸、甘氨酸和精氨酸等,其主要的水解产物是乙酸和NH
3[26,27]。可以看到,随着系统有机负荷升高,在系统失稳阶段,参与蛋白质和氨基酸物质转化的菌属相对丰度明显降低,而导致系统氨氮积累的菌属相对丰度显著升高,这与GC11和GC31系统在有机负荷为5.0 ~ 5.5 g VS/(L∙d) 时总氨氮(total ammonia nitrogen, TAN)浓度升高相对应
[16]。