0 引言
1 实验装置与数据处理
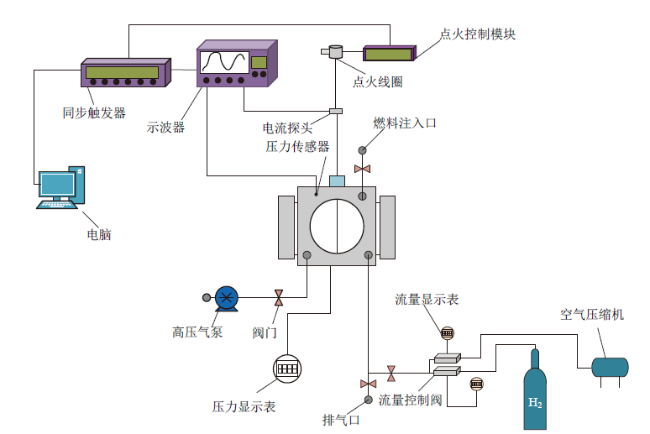
1.1 实验装置
Fig. 1 Schematic of the experiment set-up图1 实验装置示意图 |
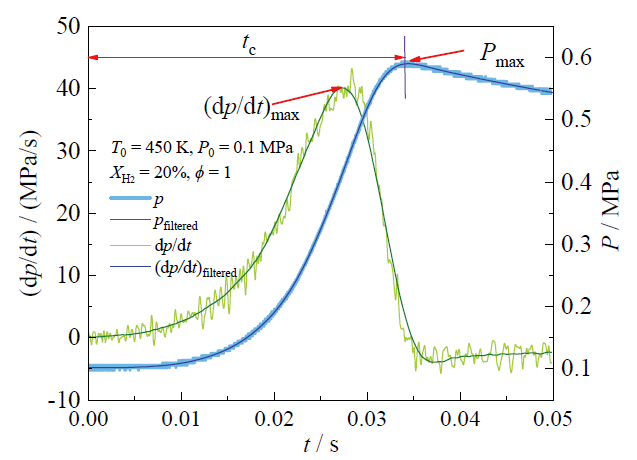
1.2 数据处理
Fig. 2 Acquisition of explosion parameters图2 爆炸参数的采集 |
2 结果与讨论
2.1 爆炸压力和压力上升率
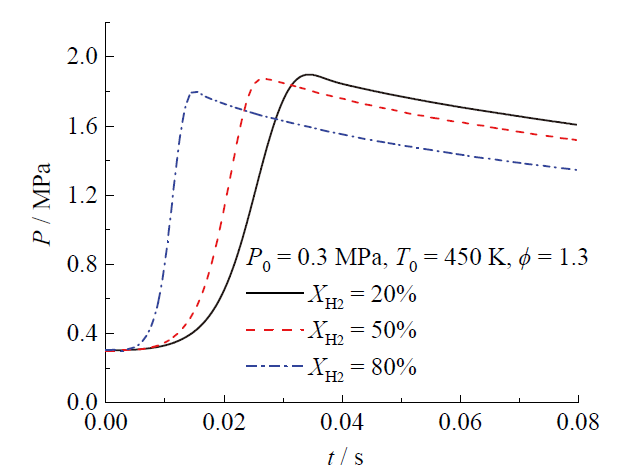
Fig. 3 C2H5OH-H2-air explosion pressure curves for different XH2 at T0 = 450 K, P0 = 0.3 MPa, ϕ = 1.3图3 在T0 = 450 K、P0 = 0.3 MPa、ϕ = 1.3时不同XH2的C2H5OH-H2-空气爆炸压力曲线 |
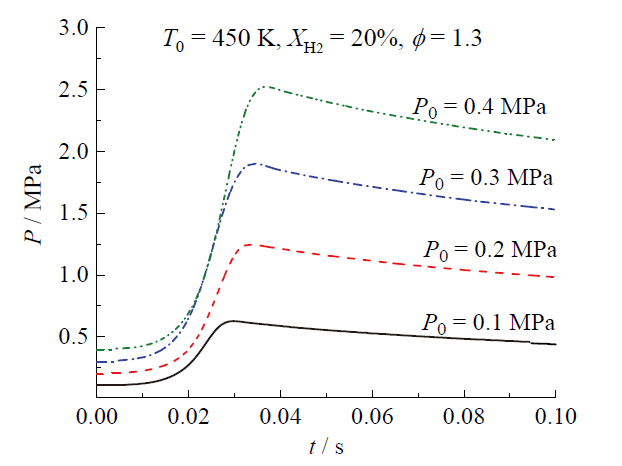
Fig. 4 C2H5OH-H2-air explosion pressure curves for different P0 at T0 = 450 K, XH2 = 20%, ϕ = 1.3图4 在T0 = 450 K、XH2 = 20%、ϕ = 1.3时不同P0下的C2H5OH-H2-空气爆炸压力曲线 |
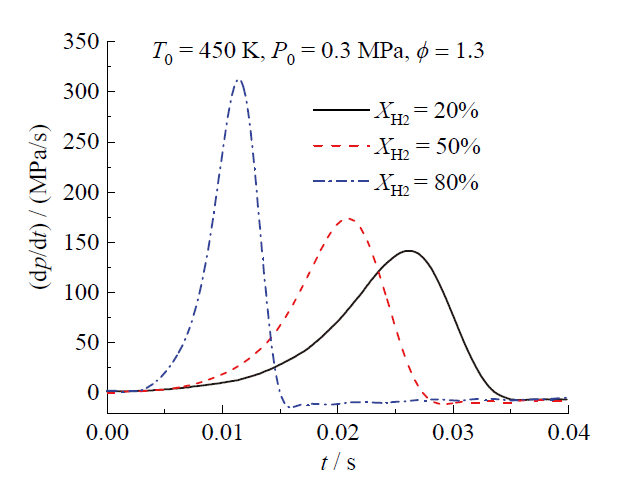
Fig. 5 C2H5OH-H2-air explosion pressure rise rate curves for different XH2 at T0 = 450 K, P0 = 0.3 MPa, ϕ = 1.3图5 在T0 = 450 K、P0 = 0.3 MPa、ϕ = 1.3时不同XH2的C2H5OH-H2-空气爆炸压力上升率曲线 |
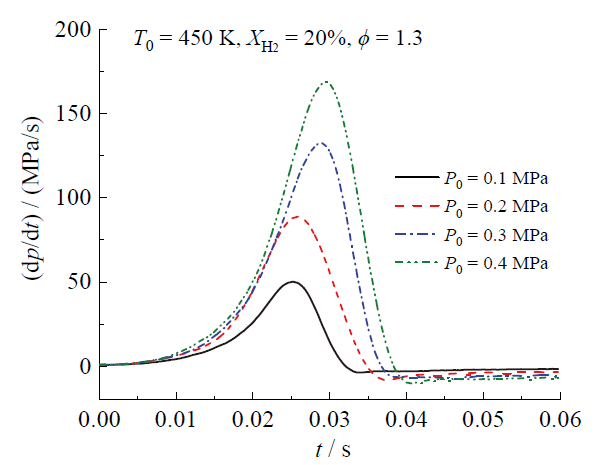
Fig. 6 C2H5OH-H2-air explosion pressure rise rate curves for different P0 at T0 = 450 K, XH2 = 20%, ϕ = 1.3图6 在T0 = 450 K、XH2 = 20%、ϕ = 1.3时不同P0下的C2H5OH-H2-空气爆炸压力上升率曲线 |
2.2 峰值爆炸压力
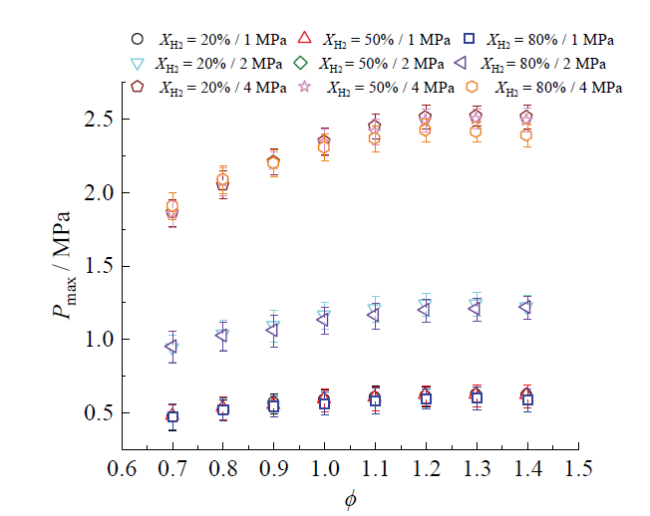
Fig. 7 Peak explosion pressure versus ϕ at XH2 = 20%-80% and P0 = 0.1 - 0.4 MPa图7 在XH2 = 20% ~ 80%和P0 = 0.1 ~ 0.4 MPa时峰值爆炸压力与ϕ的关系图 |
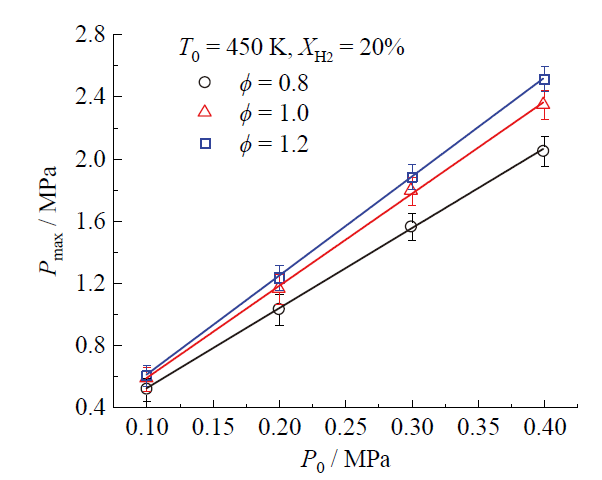
Fig. 8 Effect of P0 on peak explosion pressure at ϕ = 0.8, 1.0 and 1.2, T0 = 450 K, XH2 = 20%图8 在 ϕ = 0.8、1.0和1.2,T0 = 450 K,XH2 = 20%时,P0对峰值爆炸压力的影响 |
2.3 燃烧释放的热量
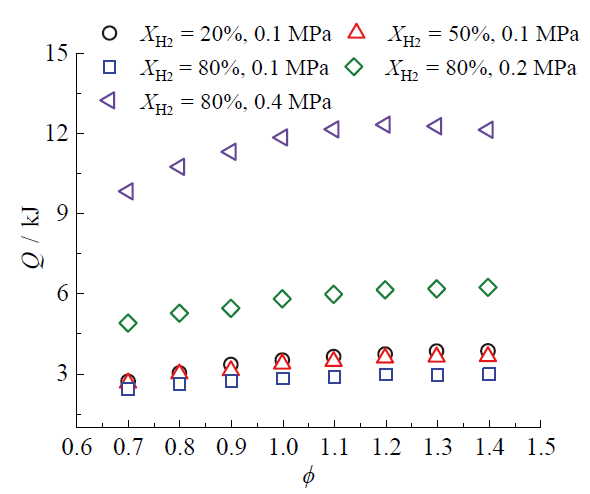
Fig. 9 The change of heat release in a fixed volume incendiary bomb with ϕ under different conditions图9 不同条件下定容燃烧弹中放热量随ϕ的变化 |
2.4 最大压力上升率和爆燃指数
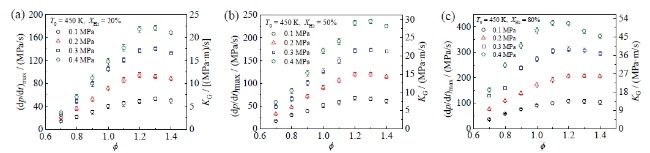
Fig. 10 The maximum explosion pressure rise rate and KG change with ϕ under different ϕ: (a) XH2 = 20%; (b) XH2 = 50%; (c) XH2 = 80%图10 不同ϕ下最大爆炸压力上升率和KG随ϕ的变化:(a)XH2 = 20%;(b)XH2 = 50%;(c)XH2 = 80% |
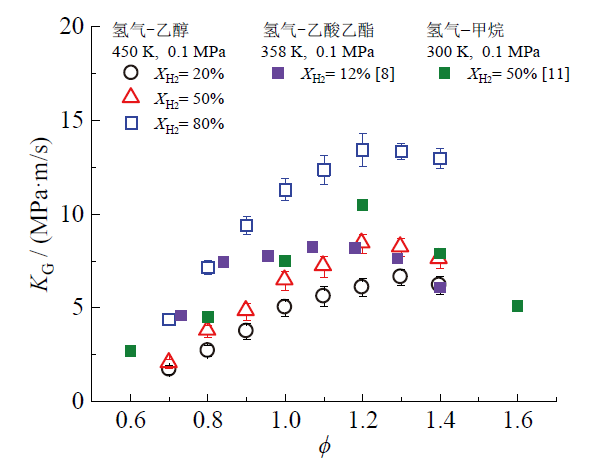
Fig. 11 The experimental KG compared with results from the references图11 KG实验结果与文献结果对比 |
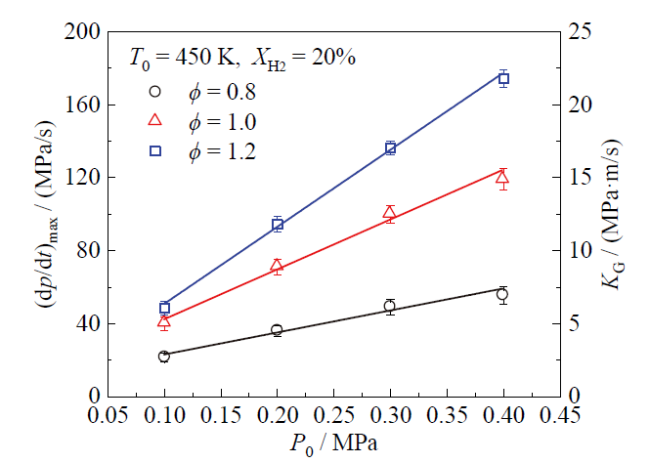
Fig. 12 The maximum explosion pressure rise rate and KG increase linearly with ϕ under different ϕ at T0 = 450 K, XH2 = 20%图12 在T0 = 450 K、XH2 = 20%时,不同ϕ下最大爆炸压力上升率和KG随ϕ变化图 |
2.5 爆炸时间
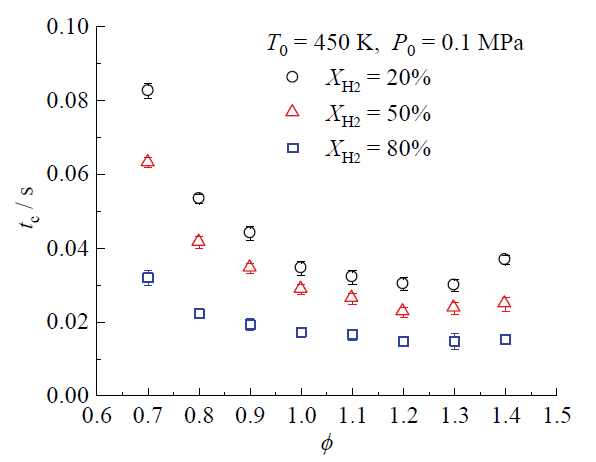
Fig.13 Variation of tc with ϕ for different XH2 at T0 = 450 K, P0 = 0.1 MPa图13 在T0 = 450 K、P0 = 0.1 MPa时,不同XH2下tc随ϕ的变化 |
2.6 动力学分析
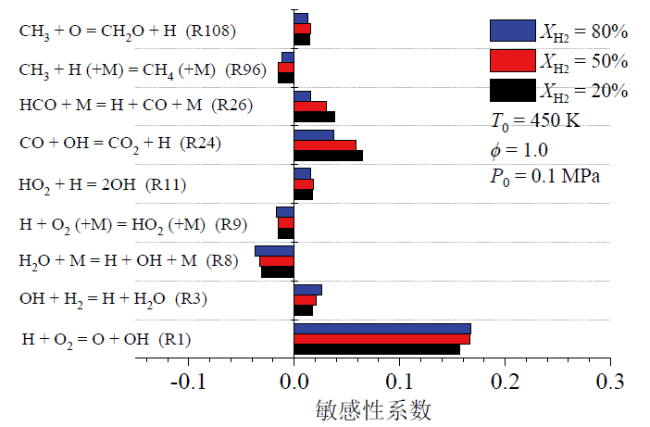
Fig. 14 Sensitivity coefficient at different XH2图14 不同XH2下的敏感性系数 |
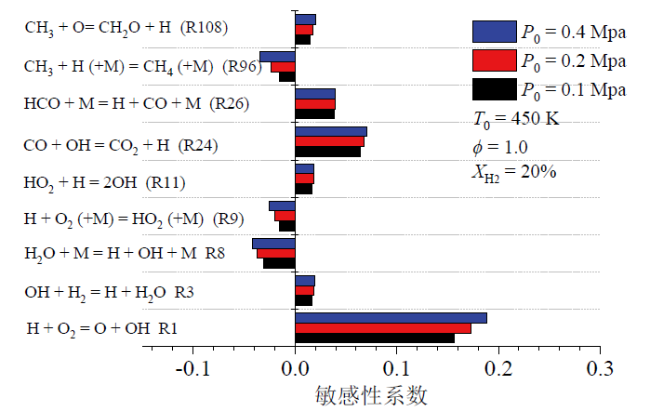
Fig. 15 Sensitivity coefficient at different P0图15 不同P0下的敏感性系数 |