0 引言
1 实验部分
1.1 实验试剂
1.2 材料合成
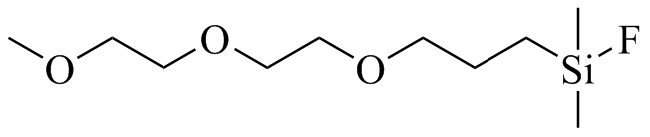
Fig. 1 Chemical structure of MFSM2图1 MFSM2化学结构式 |
1.3 材料表征
1.4 电化学测试
2 结果与讨论
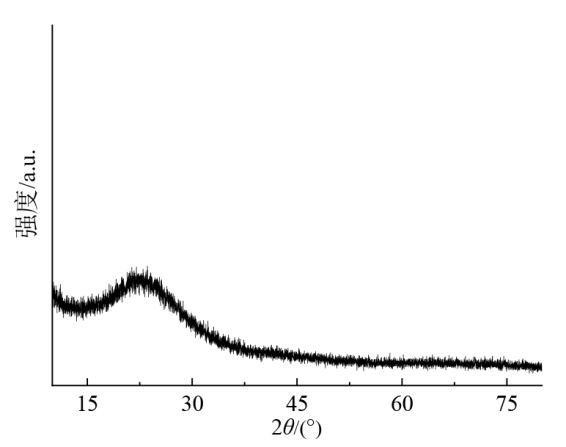
Fig. 2 XRD patterns of SiOCN图2 SiOCN的XRD图谱 |
Fig. 3 SEM image of SiOCN图3 SiOCN的SEM图像 |
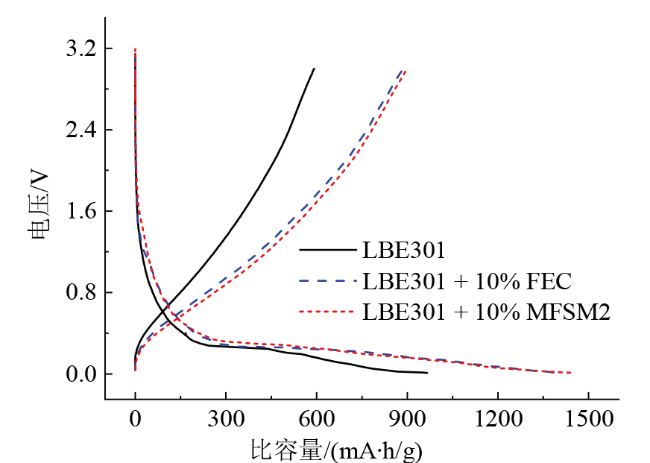
Fig. 4 Charge-discharge curves of SiOCN/Li in different electrolytes图4 SiOCN /Li在不同电解液中的充放电曲线 |
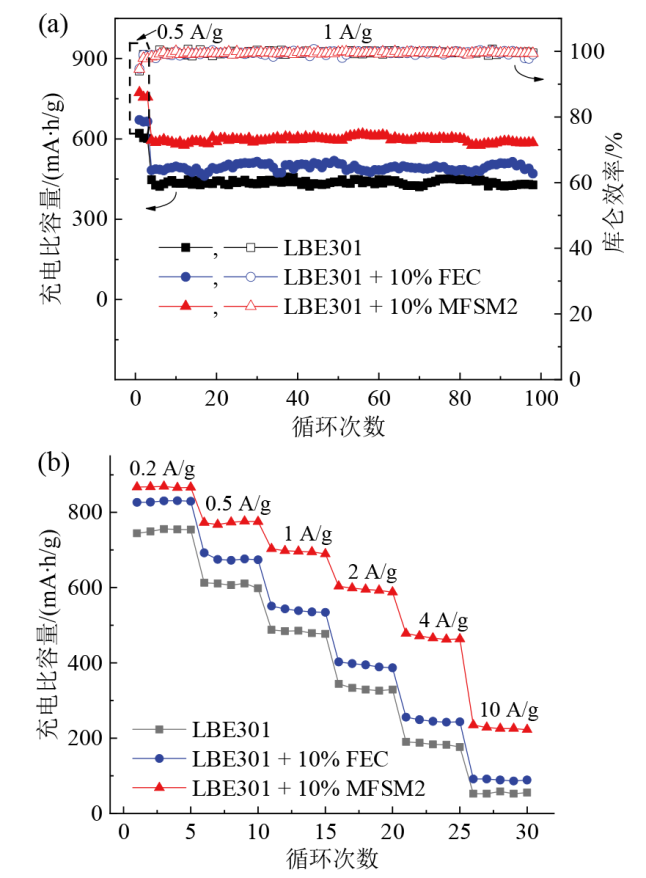
Fig. 5 Prolonged cycling performance and Coulombic efficiency (a), and rate performance (b) of SiOCN/Li half-cells with different electrolytes图5 SiOCN/Li在不同电解液中的长循环性能和库仑效率(a)及倍率性能(b) |
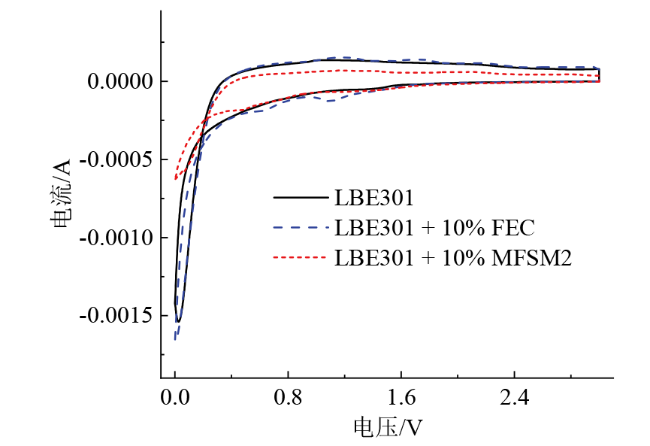
Fig. 6 CV curves of SiOCN/Li in different electrolytes图6 SiOCN/Li在不同电解液中的CV曲线 |
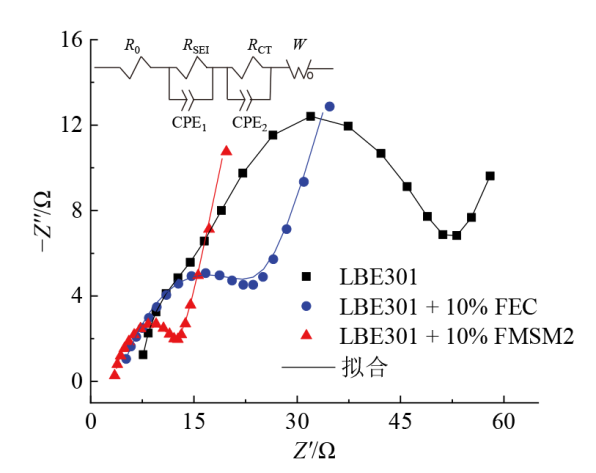
Fig. 7 EIS curves and equivalent circuit diagrams of SiOCN/Li in different electrolytes图7 SiOCN/Li在不同电解液中的EIS曲线和等效电路图 |
Fig. 8 Surface SEM plots of SiOCN anode: (a) no cycling; a long cycling with base electrolyte LBE301 (b), electrolyte with addition of 10% FEC (c), and electrolyte with 10% MFSM2 (d)图8 SiOCN负极的表面SEM图:(a)未循环;使用电解液LBE301(b)、添加10% FEC电解液(c)和添加10% MFSM2电解液(d)的长循环 |