0 引言
1 材料与方法
1.1 原料
Table 1 Composition of sludge feedstock (dry basis)表1 污泥原料组成(干基) |
| 组成 | 含量/% |
|---|---|
| C | 22.86 |
| H | 3.53 |
| O | 16.32 |
| S | 0.69 |
| N | 4.56 |
| 灰分 | 52.04 |
1.2 实验内容
1.3 分析方法
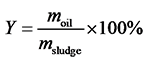
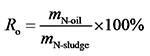
2 结果与讨论
2.1 分段水热的结果分析
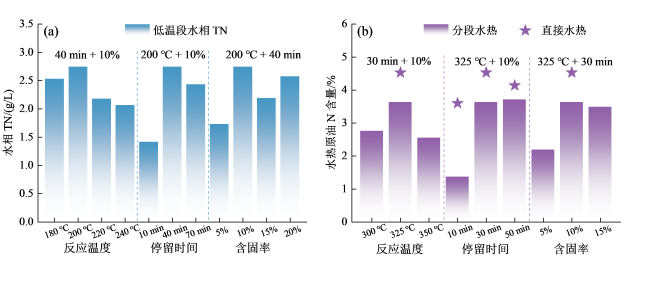
Fig. 1 Nitrogen content in products under different conditions: (a) aqueous phase; (b) hydrothermal crude oil图1 不同条件下产物中氮的含量:(a)水相;(b)水热原油 |
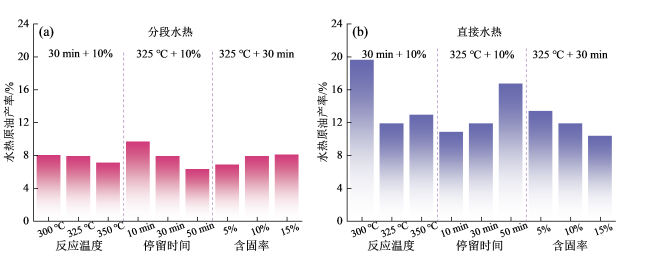
Fig. 2 Biocrude yield of hydrothermal liquefaction under different conditions: (a) stepwise hydrothermal; (b) direct hydrothermal图2 不同条件下水热原油的产率:(a)分段水热;(b)直接水热 |
2.2 分段水热的氮组分分析
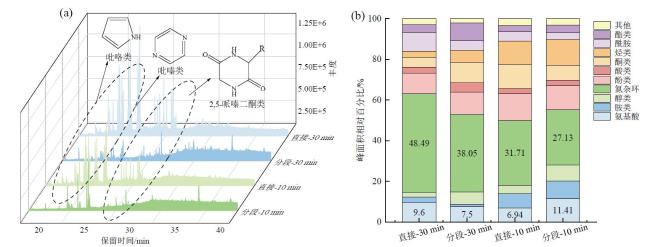
Fig. 3 GC-MS results of biocrude: (a) chromatograms diagram; (b) relative percentage content of peak area图3 水热原油GC-MS结果:(a)色谱图;(b)峰面积相对百分比含量 |
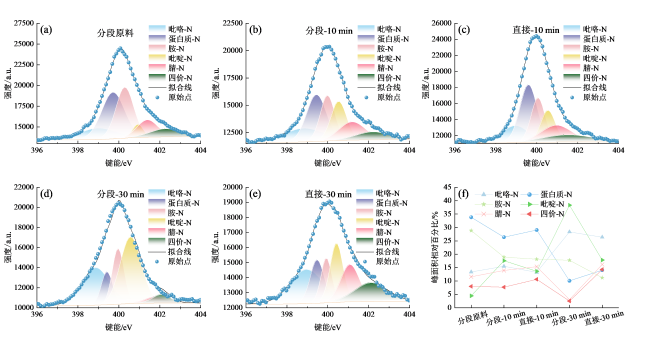
Fig. 4 XPS fitting results for hydrochar: (a-e) N 1s split-peak distribution; (f) relative percentage of peak area图4 水热炭XPS拟合结果:(a~e)N 1s分峰分布;(f)峰面积相对百分比 |
2.3 分段水热的氮平衡分析
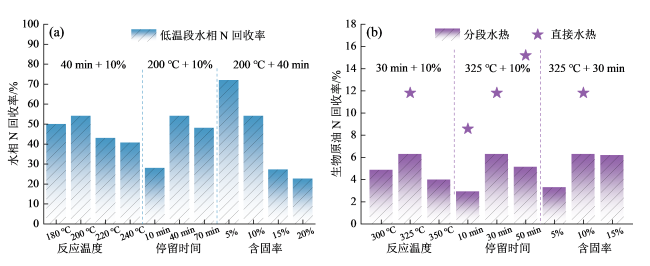
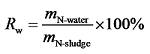
Fig. 5 Nitrogen recovery of products under different conditions: (a) aqueous phase; (b) hydrothermal crude oil图5 不同条件下产物的氮回收率:(a)水相;(b)水热原油 |
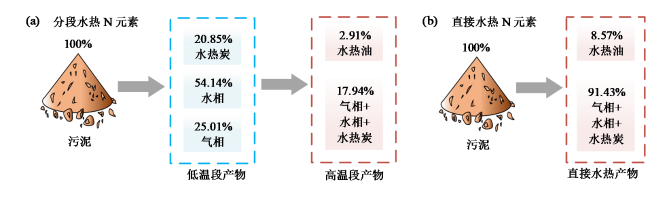
Fig. 6 Mass flow of nitrogen (325 °C + 10 min + 10%): (a) stepwise hydrothermal; (b) direct hydrothermal图6 氮元素的质量流动(325 ℃ + 10 min + 10%):(a)分段水热;(b)直接水热 |